Evaporação
Geralmente quando lavamos algo, como por exemplo, roupas, achamos que o certo é colocá-las ao Sol para que sequem mais rapidamente. Ao prepararmos um chá ou café, também percebemos que com o passar do tempo a água aquece até entrar em ebulição. Somente a partir desse momento (ebulição) é que pensamos que a água evapora. Mas aí vem a pergunta: por que as roupas secam no varal?
As roupas secam no varal pelo fato de um líquido poder passar para o estado de vapor mesmo com uma temperatura menor do que a temperatura de ebulição. Sob pressão de 1 atm, em relação ao nível do mar, a água ferve a 100ºC, no entanto essa mesma água pode passar para o estado de vapor com temperatura menor que 100ºC. Sabemos disso, pois, como citado anteriormente, as roupas molhadas colocadas no varal secam à temperatura ambiente. Esse tipo de evaporação também ocorre nos lagos, nos rio e nos mares.
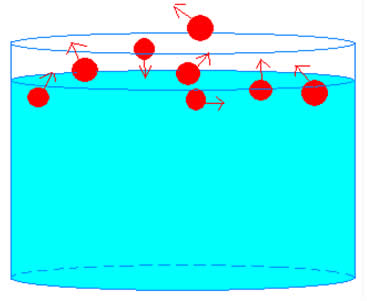
De acordo com a figura acima vemos que algumas moléculas que compõem o líquido possuem energia cinética maior do que o normal e outras possuem energia cinética menor que o normal. As moléculas com mais energia cinética conseguem escapar para o meio externo pelo fato de possuírem maior energia cinética do que outras moléculas. Quando essas moléculas escapam do líquido elas produzem uma vaporização superficial denominada evaporação.
Caso a quantidade de moléculas que deixam o líquido seja maior do que a quantidade de moléculas que entram, teremos como resultado a evaporação. Porém podemos dizer que a intensidade do processo de evaporação depende da tensão superficial do líquido.
Assim, podemos definir a evaporação como sendo uma vaporização do líquido que se dá na sua superfície livre, a uma temperatura menor do que a temperatura de ebulição. Como a evaporação decorre da grande energia cinética de algumas moléculas, ela é favorecida pelo aumento de temperatura, ou seja, quanto maior for a temperatura, maior será a intensidade da evaporação.