Segunda Lei de Soddy
A segunda lei de Soddy se refere à transformação sofrida pelo núcleo que emite partículas beta (β). Lembre-se que uma partícula beta é um elétron que foi emitido pelo núcleo atômico.
Essa lei, também conhecida como Segunda Lei da Radioatividade ou Lei de Soddy, Fajans e Russel, pode ser enunciada da seguinte forma:

Veja alguns exemplos:
146C → 0-1β + 147N
23491Pa → 0-1β + 23492U
Observe que, nos dois casos, o número de massa (A) – que fica no canto superior esquerdo – permaneceu constante. Já o número atômico (Z) – que fica no canto inferior esquerdo – aumentou uma unidade (7 =1 +6 e 92 = 1 +91).
Portanto, pode-se concluir o seguinte: os átomos X e Y são isóbaros, ou seja, possuem o mesmo número de massa e, como o número atômico de Y é maior uma unidade que o de X, ele sempre estará localizado uma casa à direita de X na tabela periódica. Veja isso na tabela periódica abaixo e relacione com os exemplos que foram apresentados acima.
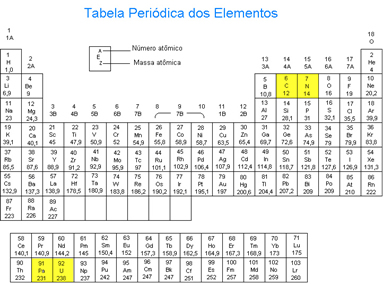
Mas surge então uma questão:
Se a partícula beta é constituída de apenas um elétron, então por que o número atômico, que é o mesmo que o número de prótons no núcleo, sofreu alteração?
A explicação foi dada pelo físico italiano Enrico Fermi (1901-1954), que propôs a seguinte hipótese:

Essa hipótese explica perfeitamente o efeito observado:
- Visto que o número de massa (A) corresponde à soma dos prótons e dos nêutrons (A = P + N) presentes no núcleo, ele permanecerá constante, pois ao mesmo tempo em que um nêutron se desintegrou, foi formado um próton; e como a massa do próton é praticamente igual à massa do nêutron, a massa total do núcleo não se altera;
- O número atômico (Z) corresponde à quantidade de prótons presentes no núcleo. Como se formou um próton, o número atômico aumenta uma unidade com a emissão da partícula beta;
- O neutrino é uma partícula subatômica de carga elétrica e massa desprezíveis, assim ele não afeta em nada na estrutura do átomo.

A comprovação da existência real do neutrino foi feita pelo físico austríaco Wolfgang Pauli (1900-1958).

