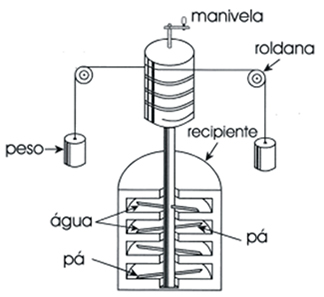
Equivalência entre Joule e Caloria
No estudo sobre trocas de calor vimos que dois ou mais corpos, com temperaturas diferentes, quando são colocados em um mesmo recipiente, o calorímetro, realizam trocas de calor entre si até que cheguem a uma temperatura em comum, isto é, até que atinjam o equilíbrio térmico.
Diz a lei geral das trocas de calor que a soma algébrica de todas as quantidades de calor trocadas entre os corpos é igual a zero, ou seja, é nula.
Quem pensa que há trocas de calor somente quando dois ou mais corpos estão isolados em um calorímetro está um pouco equivocado, pois com o atrito dos dois corpos ambos se aquecem, isto é, eles se aquecem por conta do trabalho mecânico. Quando atritamos dois corpos (trabalho mecânico), estamos produzindo os mesmos efeitos que quando fornecemos calor aos corpos.
Sendo assim, a equivalência entre as duas unidades (calor e energia mecânica) pode ser feita através da experiência de Joule. Joule realizou um experimento em que conseguiu converter energia mecânica em calor.
A atividade experimental que Joule realizou para a equivalência mecânica tinha por base os corpos em queda livre, ou seja, sujeitos apenas à ação da gravidade. Para isso, os corpos que estavam em queda moviam um conjunto de pás mergulhadas em um calorímetro com água.
Tendo conhecimento do peso de ambos os corpos, altura de queda e o equivalente em massa de água usada no calorímetro, Joule media a variação da temperatura do sistema. Através de sua experiência, ele concluiu que:
1 cal = 4,186 J