Efeito dos catalisadores sobre o equilíbrio químico

Os catalisadores são substâncias adicionadas a uma reação que ao final são reconstituídas, e, portanto, não participam da reação; porém, eles possuem a capacidade de aumentar a velocidade da reação. Isso ocorre porque os catalisadores modificam os mecanismos das reações e diminuem a energia de ativação, isto é, a energia mínima necessária para que a reação ocorra.
Com a diminuição dessa energia, que funciona como uma espécie de “obstáculo”, a reação se processa mais rapidamente. No entanto, o catalisador não aumenta o rendimento ou quantidade de produtos das reações, mas permite que sejam produzidos mais rapidamente.
Observe abaixo uma reação reversível em equilíbrio com e sem catalisador:
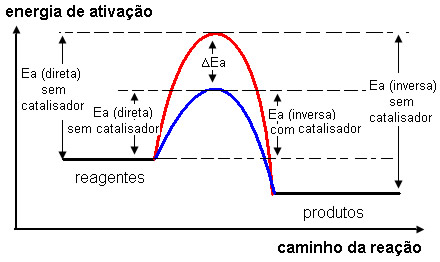
Observe que, tanto a reação direta, como a inversa, são afetadas da mesma forma pelo catalisador. Em equilíbrio, a diminuição da energia de ativação, produzida pelo catalisador, tem o mesmo valor para a reação direta e para a inversa. Isso significa que os catalisadores não deslocam os equilíbrios químicos.
O único efeito dos catalisadores é diminuir o tempo para que o sistema entre em equilíbrio. Por exemplo, em uma reação entre 3 mol de ácido etanoico (CH3COOH)e 3 mol de etanol (CH3CH2OH), se obtém 2 mol de etanoato de etila (CH3COOCH2CH3) e água. Essa reação se processa da seguinte forma sem o uso de catalisadores:
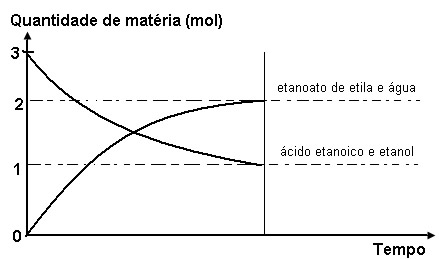
Agora observe essa mesma reação, mas com o uso de catalisador H+(aq):
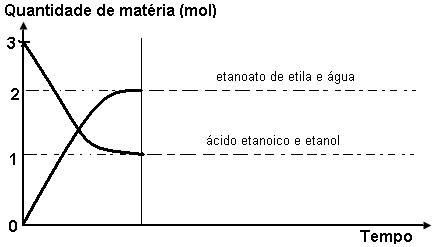
Nos dois gráficos, tanto na reação com catalisador, como a sem catalisador, o número de mol das substâncias reagentes e dos produtos no equilíbrio é igual. Entretanto, conclui-se que o tempo para se atingir o equilíbrio é menor com o uso do catalisador.
Ferramentas Brasil Escola
Artigos Relacionados

Últimas notícias
Outras matérias