Temperatura e velocidade das reações
No cotidiano podemos ver inúmeras situações em que a temperatura certamente influencia na rapidez com que as reações químicas se processam. Por exemplo, quando colocamos o feijão para cozinhar na panela de pressão, o aumento da pressão provoca o aumento da temperatura de ebulição do líquido. Assim, a reação (cozimento) ocorre com uma maior velocidade. O contrário acontece ao colocarmos os alimentos na geladeira, pois uma diminuição da temperatura faz com que a decomposição dos alimentos por microrganismos se dê de forma mais lenta.

Mas por que o aumento de temperatura aumenta a reatividade da substância?
Isso ocorre porque a temperatura é uma medida da agitação térmica das partículas que compõem uma substância. Isso significa que se aumentarmos a temperatura, a agitação das moléculas também aumentará; e o contrário também é verdadeiro: com a diminuição da temperatura, a agitação das moléculas também diminuirá.
Um aumento na agitação das moléculas faz com que elas se movimentem mais rapidamente, aumentando a probabilidade de se colidirem* de forma efetiva e com maior frequência. Como resultado, os reagentes atingirão mais rapidamente o complexo ativado que é o estado intermediário entre os reagentes e os produtos de uma reação.
Resumidamente, temos:
Isso pode ser visualizado por meio de um gráfico que relaciona a quantidade de uma fração de partículas dos reagentes (é apenas uma fração porque as energias cinéticas de todas as partículas não são iguais) em relação à energia cinética média dessas partículas, em uma determinada temperatura. Abaixo temos dois gráficos: o primeiro estabelece essa relação na reação em uma temperatura T1. Já nos segundo, observe o que ocorre quando temos uma temperatura (T2) mais elevada:
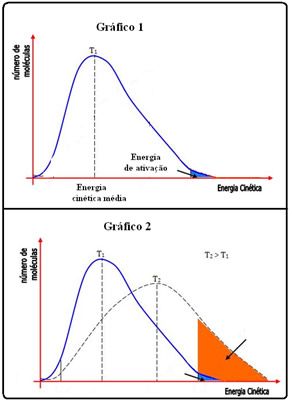
Observe que, com o aumento da temperatura, ocorre um aumento da energia cinética média das moléculas, havendo uma distribuição dessa energia. Isso faz com que haja mais moléculas com energia suficiente para reagir, o que acarreta no aumento da velocidade da reação.
O primeiro cientista que estudou essa influência da temperatura sobre a velocidade das reações foi Jacobus Vant’t Hoff, no final do século XIX. Ele chegou por meio de seus estudos à seguinte regra:

Considere uma reação que ocorre com uma velocidade V à temperatura de 5 ºC. Se aumentarmos 10ºC, indo para 15 ºC, a velocidade da reação passará a ser de 2V e assim sucessivamente.
No entanto, essa regra não se aplica a todas as reações. Por exemplo, uma exceção está demonstrada abaixo:
2 HI(g) → H2(g) + I2(g)
Se inicialmente tivermos essa reação ocorrendo a uma temperatura de 300ºC e elevarmos a temperatura para 500ºC, verificaremos um aumento na velocidade da reação de aproximadamente 25 mil vezes.
* Para um melhor entendimento sobre por que a colisão entre as partículas de uma substância é uma condição necessária para a ocorrência de uma reação, leia o texto “Teoria das colisões”.

