Isomeria de Posição
Um tipo de isomeria plana ou constitucional é a isomeria de posição ou posicional. Ela ocorre quando temos dois compostos com a mesma fórmula molecular, mesmo grupo funcional e mesmo tipo de cadeia, mas que se diferenciam na posição da insaturação, do grupo funcional, do heteroátomo ou do radical substituinte. Veja cada um desses casos:
1. Posição da insaturação:
A insaturação é uma ligação dupla ou tripla entre carbonos. Isômeros planos posicionais possuem essas ligações em diferentes posições, isto é, entre diferentes carbonos ao longo da cadeia, e para tal é necessário que esses compostos não sofram ressonância e tenham no mínimo 4 carbonos.
Exemplos:
- Fórmula molecular: C4H8
.jpg)
A dupla ligação está entre os carbonos 1 e 2 A dupla ligação está entre os carbonos 2 e 3
- Fórmula molecular: C4H6
.jpg)
A tripla ligação está entre os carbonos 1 e 2 A tripla ligação está entre os carbonos 2 e 3
- Os ácidos ômega-3 e ômega-6, presentes em peixes gordurosos como o salmão, atum e sardinha, e óleos vegetais como o de nozes, de avelã e de amêndoas, são essenciais para o organismo humano. Esses dois compostos são isômeros de posição e se diferenciam pela posição da insaturação, conforme pode ser visto abaixo:
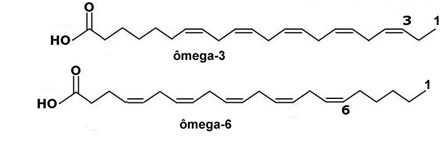
Veja que no ômega-3 a primeira ligação dupla está disposta no terceiro carbono e no ômega-6 a primeira insaturação sai do carbono 6.
Essa grande quantidade de insaturações faz com que esses ácidos graxos tenham a capacidade de combater algumas doenças do sistema circulatório, como trombose, doenças vasculares e arteriosclerose, e também processos inflamatórios, artrite e proliferação tumoral.
2. Posição do grupo funcional:
Nesse caso, o que muda é a posição em que o grupo funcional está ligado à cadeia homogênea, como os grupos dos álcoois (caracterizados pela hidroxila) e das cetonas (caracterizados pelo grupo carbonila entre dois carbonos).
Exemplos:
- Fórmula molecular: C3H8O (grupo funcional: álcool)
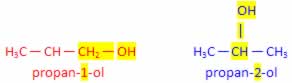
Ponto de fusão e ebulição: -126ºC e 96 ºC Ponto de fusão e ebulição: -86ºC e 82,5 ºC
A hidroxila está ligada ao carbono 1 A hidroxila está ligada ao carbono 2
- Fórmula molecular: C5H10O (grupo funcional: cetona)
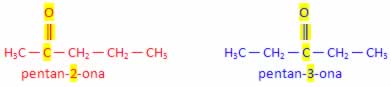
O grupo funcional (carbonila) O grupo funcional (carbonila)
está no carbono 2 está no carbono 3
3. Posição de um heteroátomo:
Heteroátomo é todo elemento que aparece entre dois carbonos na cadeia. Assim, geralmente nos ésteres, éteres, aminas e aminas, aparecem os heteroátomos oxigênio (O) e o nitrogênio (N) em diferentes posições.
Exemplos:
- Fórmula molecular: C4H10O (grupo funcional: éter)

Utilizado como anestésico comum Utilizado em sínteses industriais
O heteroátomo está entre os carbonos 2 e 3 O heteroátomo está entre os carbonos 1 e 2
- Fórmula molecular: C3H6O2 (grupo funcional: éster)
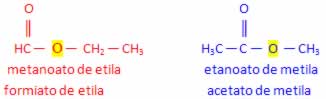
O heteroátomo está entre os carbonos 1 e 2 O heteroátomo está entre os carbonos 2 e 3
- Fórmula molecular: C3H7ON (grupo funcional: amida)
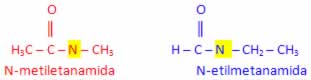
4. Posição de um substituinte (radical):
Ocorre em compostos acíclicos com no mínimo 6 átomos de carbono ou em compostos cíclicos com no mínimo 5 átomos de carbono.
Exemplos:
- Fórmula molecular: C7H16 (hidrocarboneto acíclico)
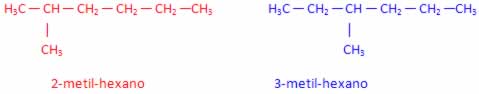
A ramificação está saindo do carbono 2 A ramificação está saindo do carbono 3
- Fórmula molecular: C7H8O (fenol)
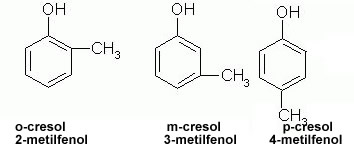
- Fórmula molecular: C5H10 (hidrocarboneto cíclico)


