A primeira lei para processos adiabáticos
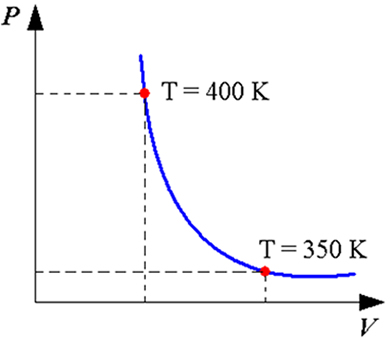
Nos estudos sobre termologia, vemos que em um processo adiabático não ocorre transferência de calor entre o meio e o sistema. Este tipo de situação é muito comum em sistemas isolados, como uma garrafa térmica ou um gás que se expande livremente, ou processos muito rápidos durante os quais não há tempo para o sistema trocar calor com o meio. A figura acima mostra o diagrama P x V para um processo adiabático.
Como não há a troca de calor, Q = 0, a Primeira Lei fica:
Q=τ+∆U
como Q=0,temos ∆U=-τ
A soma do trabalho efetuado pelo sistema com a sua energia interna é zero. Neste caso, se o volume do sistema aumentar, ou seja, se o trabalho for positivo, a sua energia deve diminuir, portanto, sua temperatura diminui. Um gás em expansão livre irá baixar sua temperatura e sua pressão.
Para um gás ideal monoatômico em um processo adiabático, a variação da energia interna será:
.jpg)
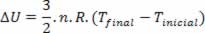
E o trabalho será:
τ=-∆U
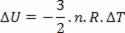
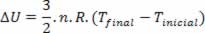
Se o gás se expandir adiabaticamente, como ocorre com o gás que sai pela válvula de um spray, por exemplo, o trabalho τ é positivo (volume aumenta), portanto ΔT deve ser negativo, ou seja, a temperatura diminui. Por isso, a temperatura de um jato de spray é menor do que a temperatura do ambiente