Densidade da água e do gelo
A água é o recurso natural mais abundante no planeta Terra, sendo que aproximadamente 70% de sua superfície é coberta por ela, dando um volume estimado de 1,4 bilhões de km3. Esse recurso é também de fundamental importância para a manutenção da vida no nosso planeta e para o desenvolvimento de nossa sociedade.
As propriedades físicas e químicas da água não se igualam às propriedades de nenhum outro líquido e são elas que a tornam tão indispensável. Entre essas características peculiares da água está a sua densidade no estado líquido e no estado sólido, isto é, na forma de gelo.
A densidade (d) é uma grandeza que mede a relação entre a massa (m) de um corpo e o volume (V) por ele ocupado, sendo calculada pela fórmula:
densidade = massa ou d = m
volume V
Geralmente, quando está no estado sólido, a substância se apresenta mais densa que no estado líquido. No entanto, é exatamente o contrário o que acontece com a água. Quando líquida e em temperatura ambiente (cerca de 20ºC), a sua densidade é aproximadamente igual a 0,99 g/cm3. Ela atinge a sua densidade máxima em aproximadamente 4ºC, que é de 1,000 g/cm3. Mas quando passa para o estado sólido, com temperaturas de 0ºC ou menos, sua densidade diminui para cerca de 0,92 g/cm3.
Visto que o gelo é menos denso que a água, ele flutua sobre ela, conforme pode ser visto na imagem do copo abaixo e também no caso dos icebergs, imensos blocos de gelo formados por água pura, que flutuam sobre os oceanos de água salgada, que é ainda mais densa por causa dos sais dissolvidos.

A densidade do gelo é menor que a da água líquida porque, conforme é bem sabido, as moléculas de água são formadas por dois átomos de hidrogênio ligados a um átomo de oxigênio, isto é, H2O. Visto que o oxigênio é mais eletronegativo que o hidrogênio, ele atrai mais intensamente o par de elétrons para si, criando uma região com maior carga elétrica na molécula. Com isso, a molécula de água é polar, com uma região parcialmente negativa e outra positiva.
Assim, a região negativa de uma molécula atrai a região positiva de outra e vice-versa, criando interações intermoleculares bem intensas, denominadas ligações de hidrogênio.
.jpg)
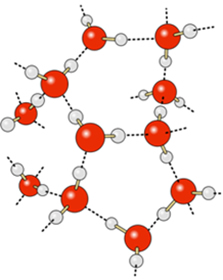
No estado líquido, as moléculas estão mais afastadas umas das outras, mas à medida que vão congelando, as moléculas se aproximam mais e formam mais ligações de hidrogênio, adquirindo uma organização específica (hexagonal) com espaços vazios. Esses espaços são os responsáveis pela expansão da água.
Visto que o volume aumenta, mas a massa de água permanece a mesma, a densidade do gelo diminui:
↓d = m
v↑
- Importância da diferença de densidade entre a água e o gelo:
Em virtude dessa diferença de densidade, as águas dos lagos e mares não se congelam completamente, pois forma-se uma camada de gelo menos densa que fica na superfície e cria um isolante térmico natural que faz com que a água abaixo dela permaneça na fase líquida. Isso salva a vida animal e vegetal dos lagos e mares.

O gelo funciona como um isolante térmico porque o seu calor específico (2,03 J/g . ºC) é menor que o da água (4,18 J/g . ºC). É por isso que os esquimós usam o gelo na construção de iglus.

Depois que o frio passa e vem a época de calor, o gelo da superfície se derrete facilmente. Mas isso não aconteceria se o gelo descesse para o fundo dos lagos e mares. Com isso, a vida animal e vegetal estaria comprometida.
Outro ponto importante é que, conforme já dito, a água líquida atinge a sua densidade máxima em aproximadamente 4ºC, que é de 1,000 g/cm3. Portanto, durante épocas como a primavera e o outono, a água atinge temperaturas próximas a essa e se torna mais densa que o restante, indo para o fundo. Isso causa um movimento vertical denominado de corrente de convecção, que é o responsável por misturar os nutrientes dissolvidos na água.


