Histórico das Primeiras Tabelas Periódicas

Muitas atividades no nosso cotidiano se repetem periodicamente, por exemplo: normalmente, estudamos de segunda a sexta-feira e, em algumas escolas, toda sexta-feira tem alguma verificação de aprendizagem. Dessa forma, dizemos que a verificação de aprendizagem se repete periodicamente, ou seja, se repete regularmente em função de um determinado parâmetro. Cada intervalo de repetição, que nesse caso é uma semana ou sete dias, é denominado período.
Outro aspecto importante que vemos em nosso dia a dia é a organização. Por exemplo, fica muito mais fácil achar um CD, se todos os CDs estiverem organizados de acordo com o tipo musical.
De maneira similar, os cientistas notaram que os elementos químicos até então conhecidos podiam ser organizados de maneira que algumas de suas características se repetissem periodicamente. Isso era de extrema importância, pois auxiliaria o estudo dos elementos, ou seja, seria mais fácil prever suas propriedades, comportamentos e até como seriam determinados elementos que nem eram conhecidos na época.
Muitas foram as tentativas de encontrar uma Tabela Periódica que organizasse os elementos químicos de forma que suas características se repetissem periodicamente.
Conforme sabemos, a que se mostrou mais coesa, a princípio, foi a de Dimitri Ivanovich Mendeleyev (1834-1907), em que as propriedades dos elementos eram consideradas funções periódicas das massas atômicas dos elementos.
Porém, em 1913, Moseley provou que as propriedades dos elementos variam periodicamente em função dos prótons existentes no núcleo dos átomos dos elementos (carga nuclear), que passou a ser denominado Número Atômico (Z). Essa ficou sendo a Tabela Periódica atual.
Entretanto, houve muitas outras tentativas que ajudaram no progresso do conhecimento da periodicidade dos elementos e que culminaram na Tabela Periódica atual. A seguir, três dessas ideias serão explanadas:
• Tríades: proposta por Johann Wolfgang Döbereiner (1780-1849), em 1817. Os elementos com propriedades semelhantes, ou seja, que reagiam de maneira semelhante com outros elementos, eram organizados em grupos de três:

Observe como esses grupos naturais aparecem na Tabela Periódica atual:
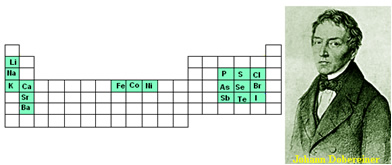
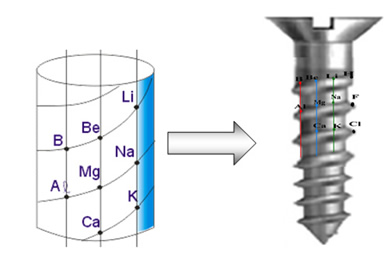
• Parafuso Telúrico: criado em 1862, por Alexandre Béguyer de Chancourtois (1819-1886). Os elementos eram agrupados em ordem crescente de massa atômica em formato de um parafuso, ou seja, na forma de um espiral de 45°, em que havia 16 elementos em cada volta. Os elementos com características semelhantes ficavam um embaixo do outro.
Por exemplo, abaixo se exibe o Boro (B) alinhado com o Alumínio (Al) e hoje esses dois elementos pertencem a mesma família (família 3 ou III A) da Tabela Periódica.
• Lei das Oitavas: essa foi proposta por John A. R. Newlands (1837-1898), em 1864. Ele colocou os elementos agrupados de sete em sete, em ordem crescente de massa atômica, e observou que o primeiro elemento tinha propriedades semelhantes ao oitavo, e assim por diante. Ele chamou de Lei das oitavas porque as características se repetiam de sete em sete, como as notas musicais.

Ferramentas Brasil Escola

Últimas notícias
Outras matérias