Influência da superfície de contato na velocidade das reações

O que enferruja mais depressa: uma palha de aço ou um prego?
Sabemos que a palha de aço enferruja com mais rapidez, porém, por que isso ocorre, se o constituinte principal em ambos os casos é o ferro?
Para responder essa pergunta devemos analisar um fator muito importante que influencia na velocidade das reações, que é a superfície de contato.
Uma reação química ocorre em virtude das colisões entre as partículas da superfície do material, assim, quanto maior for a superfície de contato dos reagentes envolvidos, maior será a taxa de desenvolvimento da reação e vice-versa.
Isso significa que com uma superfície de contato maior, haverá mais partículas entrando em colisão e aumentará a probabilidade desses choques serem efetivos, ou seja, de resultarem na quebra das ligações dos reagentes e na formação de novas ligações, originando os produtos.
Assim, podemos entender porque a palha de aço enferruja mais rápido que o prego: ela possui maior superfície de contato com o oxigênio do ar, o que acelera a reação de oxidação.
Isso também pode ser verificado em outros casos: se colocarmos um comprimido efervescente intacto em um recipiente com água, e em outro frasco com água colocarmos um comprimido transformado em pó, observaremos que o que foi adicionado em pó reagirá bem mais rápido, pois os grãos oferecem maior superfície de contato com a água.

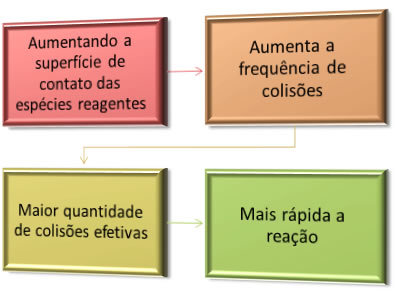
Resumidamente, temos:
Ferramentas Brasil Escola

Artigos Relacionados

Últimas notícias
Outras matérias