Polaridade dos compostos orgânicos
Polaridade é a capacidade que as ligações possuem de atrair elétrons. Quando este conceito é aplicado aos compostos orgânicos, o tipo de ligação presente é que dita a regra.
A ligação covalente é a que se faz presente na maioria das substâncias orgânicas, ela torna o composto apolar. As estruturas dos compostos orgânicos não permitem outra classificação, uma vez que correspondem às ligações formadas pela união de carbonos (C-C) e hidrocarbonetos (carbono e hidrogênio ligados). A explicação vem do fato de que a ligação ocorre entre elementos iguais, portanto possuem mesma escala de eletronegatividade.
Nem todos os compostos orgânicos são constituídos somente por carbono e hidrogênio, alguns possuem elementos diferentes ligados à cadeia carbônica, como por exemplo: Oxigênio. Dessa forma surgem as hidroxilas, formadas por oxigênio e hidrogênio (O-H).
A molécula onde a hidroxila se faz presente apresenta polaridade. Veja exemplos de compostos apolares e polares:
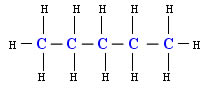
Molécula apolar
A estrutura acima corresponde ao composto orgânico Pentano, repare que os átomos ligantes são iguais (5 carbonos ligados entre si).
.jpg)
Molécula polar
A presença de outros átomos (Oxigênio ligado a hidrogênio) entre carbonos dá à molécula caráter polar. O composto acima é conhecido por três nomenclaturas diferentes: Etanol, álcool etílico ou álcool comum.
