Pressão Osmótica

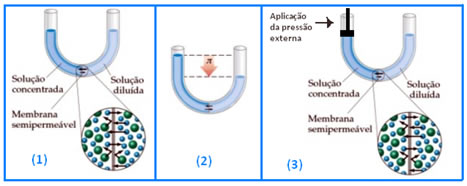
No caso abaixo temos um tubo em U, com duas soluções de concentrações diferentes separadas por uma membrana semipermeável. Normalmente, como se pode ver no quadradinho 1, o que aconteceria é que, por meio do processo de osmose, passaria a haver um desnível, pois o solvente seria transportado da solução mais diluída para a menos diluída, com o objetivo de igualar suas concentrações.
Com o passar do tempo, esse transporte cessaria, porque atingiria uma altura que geraria uma pressão hidrostática sobre a membrana, impedindo o fluxo do solvente por ela (quadrinho 2). Essa é a pressão osmótica.
Porém, se desde o início aplicássemos uma pressão sobre a solução mais concentrada ou menos diluída (a da esquerda), isso impediria que o solvente da outra solução passasse pela membrana semipermeável, ou seja, a osmose não teria ocorrido, conforme pode ser visualizado no terceiro quadrinho. Desse modo, estaríamos aplicando também uma pressão osmótica.
A pressão osmótica é simbolizada pela letra grega pi (π) e pode ser determinada por meio de duas expressões matemáticas:

Onde:
M = molaridade da solução (mol/L);
R = constante universal dos gases perfeitos, que é igual a 0,082 atm . L. mol-1. K-1 ou 62,3 mm Hg L. mol-1. K-1;
T = temperatura absoluta, dada em Kelvin;
C = concentração do soluto (mol/L);
i = fator de Van’t Hoff.
Conforme se verifica na fórmula, quanto maior a diferença de concentração entre os meios, maior será a pressão osmótica exercida.
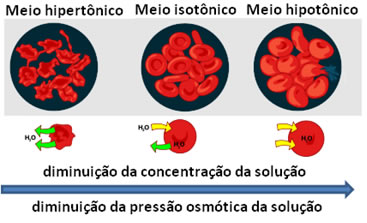
A importância da pressão osmótica pode ser vista no sangue humano. A pressão osmótica normal do sangue é de aproximadamente 7,7 atm, assim como a pressão osmótica das hemácias (glóbulos vermelhos) também é do mesmo valor. Quando isso ocorre, dizemos que o meio é isotônico (isso significa “igual”, ou seja, é isotônico quando substâncias apresentam pressões osmóticas iguais). Isso permite que as moléculas de água entrem e saiam dos glóbulos vermelhos com a mesma facilidade, garantindo seu funcionamento normal.
No entanto, se o meio for hipotônico, isto é, mais diluído que dentro da hemácia, a água passará com maior facilidade para dentro dela, fazendo com que ela inche e venha até a explodir (hemólise). Já se o meio for hipertônico, mais concentrado que dentro da hemácia, ela murchará, pois perderá água.
É por isso que o soro fisiológico usado é uma solução de NaCl que contém 0,9% em massa (ou seja, a cada 100 ml da solução aquosa há 0,9 grama do sal) ou 0,15 mol/L. Desse modo, o soro é isotônico em relação às células sanguíneas e aos líquidos corporais. Do contrário, isso afetaria de maneira grave o organismo do paciente.