Transformação isocórica ou isovolumétrica
| Uma transformação isocórica, também denominada transformação isovolumétrica, ou ainda isométrica, ocorre quando se mantém o volume constante e se variam a temperatura e a pressão de um gás com massa fixa. |
O termo isocórica vem do grego: iso significa igual, e coros é volume; isto é, volume igual ou volume constante.
Dois cientistas franceses, Jacques Alexandre César Charles e Joseph Louis Gay-Lussac, estudaram como diversos gases se comportam quando a pressão e a temperatura variam. Ambos chegaram à mesma conclusão, assim, criou-se a seguinte lei:
| Lei de Charles ou Lei de Charles e Gay-Lussac: para uma massa fixa de gás, mantida à volume constante, a pressão exercida pelo gás é diretamente proporcional à temperatura absoluta. |
Isso quer dizer que se aumentarmos a temperatura, a pressão dentro do recipiente que contém o gás irá aumentar e vice-versa. Isso ocorre porque a pressão é resultado das colisões das partículas do gás com as paredes do recipiente, assim, quanto mais colisões, maior será a pressão. Se a temperatura aumentar, a energia cinética das partículas também aumentará e elas se movimentarão com maior velocidade, aumentando a pressão.
Isso pode ser visto nos pneus de carros, motos e caminhões. Com um aumento de sua temperatura, a pressão dentro dos pneus aumenta. Por isso é necessário calibrar constantemente os pneus, ou seja, regular os níveis da pressão provocada pelos gases que os enchem. Isso garante seu melhor desempenho e também a segurança dos passageiros.
Em uma corrida, a volta de apresentação dos carros não acontece somente para mostrar os competidores e as suas “máquinas”, mas para aquecer os pneus, assim as moléculas dos gases atingem uma temperatura certa para dar a pressão ideal para a corrida.

A volta de apresentação serve para aquecer os pneus dos carros e, assim, atingir a pressão ideal para seu melhor desempenho.
Matematicamente, a Lei de Charles e Gay-Lussac é expressa por:
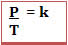
Logo, conclui-se que:
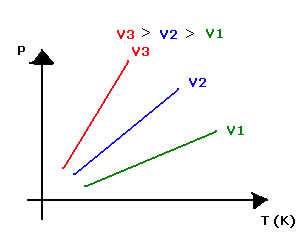
.jpg)
Seu gráfico é uma reta. No caso abaixo temos a comparação de três transformações isocóricas, sendo que cada uma foi com um volume diferente: