A Ponte Salina das Pilhas
O bom funcionamento de uma pilha depende, entre outros fatores, da existência de uma ponte salina. Mas, para entendermos por que sua presença é essencial, vejamos um exemplo de pilha e o que ocorreria com ela se não houvesse a ponte salina.
Temos abaixo uma pilha formada por um eletrodo de cobre metálico e outro de zinco mergulhados, respectivamente, em soluções de sulfato de cobre (CuSO4) e de sulfato de zinco (ZnSO4).
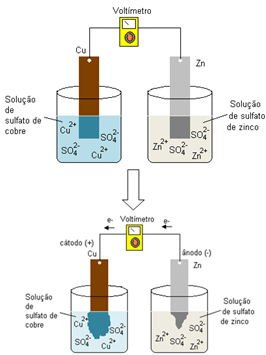
O ânodo é o zinco metálico que se oxida, liberando elétrons que são transferidos por meio do circuito elétrico externo para o cátodo (íons cobre), segundo as semirreações abaixo:
Semirreação no ânodo: Zn( s) ↔ Zn2+(aq) + 2 e-
Semirreação no cátodo: Cu2+(aq) + 2 e- ↔ Cu( s)
Reação Global: Zn( s) + Cu2+(aq) ↔ Zn2+(aq) + Cu( s)
Com o tempo, a massa da placa de zinco irá diminuir e a concentração de íons zinco (Zn2+(aq)) na solução aumentará cada vez mais. No outro eletrodo, a massa da placa de cobre irá aumentar e a concentração dos íons cobre em solução (Cu2+(aq)) diminuirá, perdendo a sua coloração azul.
Portanto, a neutralidade de ambas as soluções seriam perdidas, a solução ficaria instável devido ao excesso de cargas, o que faria a pilha parar imediatamente de funcionar.
Para solucionar esse problema, usamos a ponte salina. Ela pode ser um tubo em U que contém uma solução aquosa concentrada de um sal bastante solúvel, que liga as duas semicelas. Geralmente, as soluções usadas são de cloreto de potássio (KCl(aq)), nitrato de amônio (NH4NO3(aq)), nitrato de sódio (NaNO3(aq)) ou nitrato de potássio (KNO3(aq)). As extremidades do tubo são fechadas por algum material poroso, como algodão ou ágar-ágar.
Assim, os íons presentes na ponte salina são transferidos para ambas as soluções, mantendo-as neutras. Por exemplo, se usarmos uma solução de cloreto de potássio (KCl(aq)) com íons K+(aq) e Cl-(aq) dispersos, de modo que os os ânions Cl-(aq) sejam transferidos para a solução com excesso de íons Zn2+(aq) e os cátions K+(aq) sejam transferidos para a solução que está com poucos cátions Cu2+(aq).
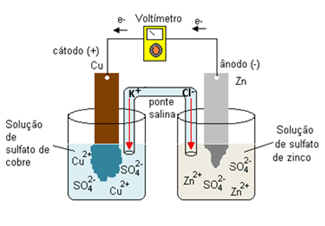
Dessa forma, ambas as soluções serão neutralizadas e o funcionamento da pilha será prolongado. No lugar da ponte salina, pode ser usado também uma placa de porcelana porosa que tem essa mesma finalidade: escoar íons entre as soluções para que elas permaneçam neutras.

