Explicação Teórica da Regra de Markovnikov
.jpg)
Em reações de adição com água, ou seja, de hidratação, esta regra também se aplica.
Isso acontece porque esses tipos de reações ocorrem na verdade com duas etapas diferentes, a lenta e a rápida, conforme mostrado abaixo. Na etapa lenta o alceno doa um par de elétrons para o próton (H+) do haleto, formando um carbocátion, uma molécula eletropositiva e um íon do halogênio (X-, onde X= Br, Cl ou I). Por ter uma energia de ativação muito alta, essa etapa é lenta e é considerada determinante para a reação.
Na segunda etapa, o carbocátion reage com o íon haleto, gerando um haleto de alquila, conforme pode ser visualizado no esquema abaixo:
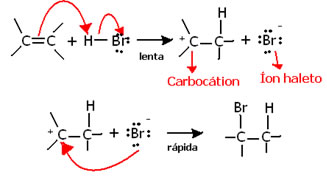
Desse modo, a estabilidade do carbocátion formado é que definirá onde o hidrogênio irá se ligar. Por exemplo, em uma molécula assimétrica há a possibilidade de formação de mais de um carbocátion. Observe abaixo:
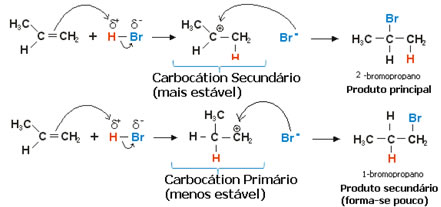
Observe que na hidro-halogenação do propeno é possível haver a formação de dois tipos de carbocátion, porém o carbocátion secundário é mais estável, sendo formado mais rapidamente. Além disso, sua energia livre de ativação é bem menor que a do carbocátion primário, sendo necessário, portanto, menos energia para a sua formação, por isso ele predomina.
Assim, o carbocátion mais estável fornece o produto mais estável, que será o produto principal da reação. Vendo por esse ângulo dos mecanismos das reações, a regra de Markovnikov pode ser enunciada mais corretamente da seguinte forma:
.jpg)