Forças ou ligações dipolo-dipolo
Existem três tipos de forças intermoleculares, conforme visto no texto “Classificação das forças intermoleculares”. Entre elas, as que ocupam estado intermediário em questão de força de atração, são as interações ou forças dipolo-dipolo, também denominadas ligações dipolo permanente-dipolo permanente.
Como o próprio nome diz, são interações entre moléculas que apresentam um dipolo permanente, ou seja, fazem referência a moléculas polares. Moléculas polares são aquelas que apresentam uma distribuição não uniforme da carga elétrica ao longo de sua superfície. Elas apresentam uma extremidade mais eletropositiva e a outra mais eletronegativa. Dessa forma, a molécula polar adquire um dipolo elétrico permanente que interage com as outras moléculas de sua vizinhança.
Isso pode ser visualizado no caso do HCl. Visto que o cloro é mais eletronegativo, ou seja, atrai com maior força o par de elétrons do que o hidrogênio, ele constitui a parte negativa da molécula. E, consequentemente, o hidrogênio é a parte positiva. Esse dipolo elétrico pode ser representado da seguinte forma:
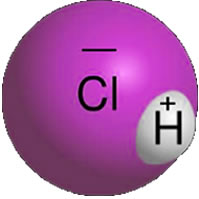
Assim, entre suas moléculas há uma atração, pois o polo positivo de uma molécula (H) atrai o negativo de outra (Cl), conforme é mostrado a seguir.
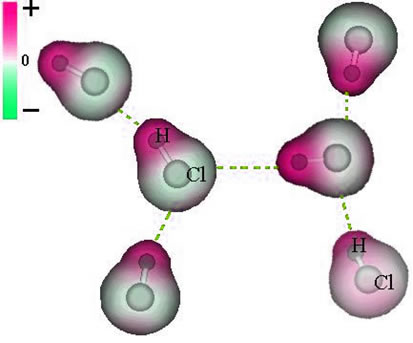
Desse modo é um dipolo permanente de uma molécula sendo atraído pelo dipolo permanente de outra. E quanto maior for a polaridade da molécula, mais intensas serão as interações dipolo-dipolo.
Em substâncias sólidas, a formação desse dipolo permanente faz com que haja a formação de cristais dipolares.
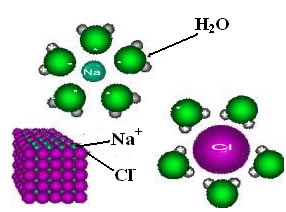
É possível também haver uma interação parecida com essa, que é a interação íon-dipolo, em que um íon é atraído por um polo de uma molécula polar. Por exemplo, ao adicionarmos cloreto de sódio, que é o sal de cozinha, na água, haverá sua dissociação iônica. O que significa que seus íons (Na+ e Cl-) serão separados. Essa separação é resultado da forte atração entre esses íons já presentes nas moléculas do sal e os polos da água, visto que ela é polar.
Quando isso ocorre, os íons ficam circundados pelas moléculas de água e dizemos que eles estão hidratados.