Ligação iônica e covalente: qual delas é polar?
Polaridade se define como a capacidade que as ligações possuem de atrair cargas elétricas, e o local onde essas cargas se acumulam é denominado de pólo, que se classifica em pólos negativos ou positivos.
Mas no que se trata de ligação iônica e covalente: como elas se classificam?
Toda ligação iônica é uma ligação polar. Os compostos iônicos são carregados de cargas elétricas positivas (cátions) e negativas (ânions) e, portanto, apresentam pólos. As substâncias iônicas se tornam instáveis, pois reagem facilmente com outros compostos.
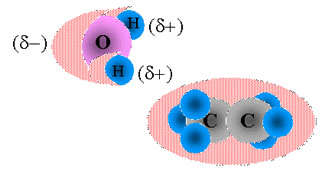
Polaridade das ligações iônica e covalente.
Como pode ser observado na figura acima, a água composta por dois átomos de Hidrogênio e um de Oxigênio é um composto polar, os sinais δ+ e δ- (pólo positivo e negativo) representam esse aspecto. Já o composto covalente C2H6 (Etano) é apolar.
Mas não significa que todo composto covalente é apolar. Os pólos neste caso estão associados à eletronegatividade. Se a ligação covalente for entre átomos de mesma eletronegatividade, como é o caso do Etano, a ligação será apolar, porque não ocorre formação de pólos.
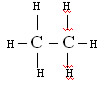
*A ligação ocorre entre elementos iguais e com mesma eletronegatividade.
Agora, se a ligação covalente ocorrer entre átomos com eletronegatividades diferentes, a ligação será polar. Essa diferença induz o acúmulo de carga negativa ao redor do elemento mais eletronegativo, gerando assim, pólos δ- na molécula. Esta regra obedece à escala de eletronegatividade de Pauling:
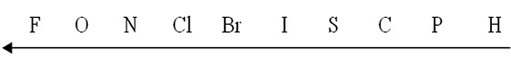
A eletronegatividade é crescente no sentido da seta. Para memorizar a escala acima, sugerimos um macete:
“Fui Ontem No Clube, Briguei I Saí Correndo Para o Hospital”.
Os elementos são representados pelas letras em destaque.
Exemplo: a molécula de ácido clorídrico é composta por hidrogênio (H) e cloro (Cl). De acordo com a escala de Pauling, o “Cl” se encontra em uma extremidade e o “H” na outra, ou seja, estão bem afastados. Por isso a molécula de HCl é classificada como polar, pois os elementos que a formam possuem eletronegatividades distintas.
δ+ δ-
H ─ Cl *Como o Cloro é mais eletronegativo, atrai para si o pólo com carga negativa.
Ferramentas Brasil Escola
Artigos Relacionados

Últimas notícias
Outras matérias