Número de nuvens eletrônicas e a hibridização
É possível definir a hibridização de um composto através da contagem do número de nuvens eletrônicas ao redor de seu átomo central.
Tabela que define a hibridização de acordo com o número de nuvens:
.jpg)
Vamos ao exemplo clássico do metano:
.jpg)
Repare que existem 4 nuvens (cor cinza) ao redor do átomo central (carbono). Dizemos que a estrutura possui geometria tetraédrica, portanto possui hibridização sp3.
As imagens a seguir são tridimensionais, elas facilitam na compreensão do número de nuvens eletrônicas, que se apresentam na cor verde.
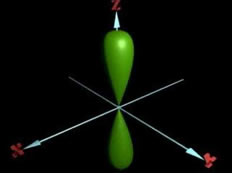
Hibridização sp: geometria linear, 2 nuvens eletrônicas
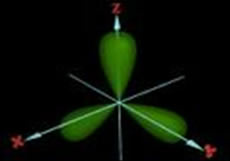
Hibridização sp2: geometria trigonal, 3 nuvens eletrônicas
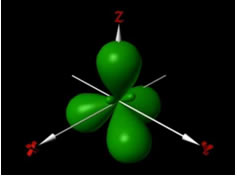
Hibridização sp3: geometria tetraédrica, 4 nuvens eletrônicas
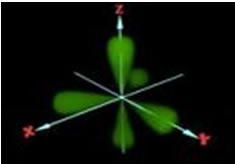
Hibridização sp3d: geometria bipirâmide de base triangular, 5 nuvens eletrônicas
Por Líria Alves
Graduada em Química
