Ácido Fluorídrico (HF)
O ácido fluorídrico é composto de um átomo de flúor e um de hidrogênio, ligados por uma ligação covalente. Ele é um líquido incolor, fumegante, de ponto de ebulição 20 ºC sob pressão normal. Portanto, nas condições ambientes, onde a temperatura é de 25 ºC, ele é um gás incolor.
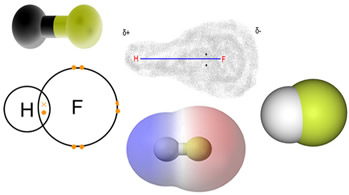
Seu ponto de ebulição é superior ao dos demais ácidos halogenídricos, isto é, daqueles formados pela ligação do hidrogênio com um halogênio (elemento pertencente à família 17 ou VII A da Tabela Periódica). Isso se deve ao fato de que há entre suas moléculas a formação de fortes ligações de hidrogênio, que é o tipo de força intermolecular mais forte. As ligações de hidrogênio criam a seguinte estrutura:
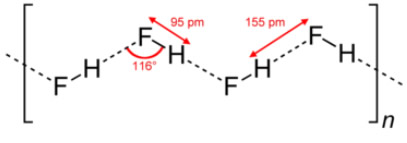
Sua principal propriedade é a de ser um elemento altamente corrosivo; sendo, por esse motivo, usado em solução aquosa para corroer o vidro, fazendo gravações como a mostrada a seguir:

Por isso, em laboratórios, o ácido fluorídrico é guardado em frascos plásticos.
Esse ácido é produzido a partir da reação do ácido sulfúrico concentrado com o minério fluorita (CaF2), à temperatura de 250 ºC:
CaF2(s) + H2SO4(l) → CaSO4(s) + 2 HF(g)

