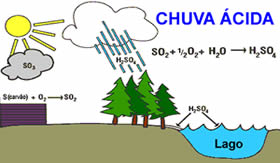
Química da chuva ácida
A formação de chuvas ácidas trata-se de um problema moderno, que teve origem a partir do grande crescimento dos centros urbanos que são altamente industrializados.
Existem diversas fontes de poluentes para a atmosfera, os gasosos são gerados pelas indústrias, veículos e usinas energéticas, exemplos: dióxido de enxofre e óxido de nitrogênio. A combinação desses poluentes com o vapor de água existente na atmosfera vai se acumulando em nuvens ocorrendo assim sua condensação, da mesma forma como são originadas as chuvas comuns.
Na natureza, a água reage com certos óxidos formando ácidos. O ácido carbônico (H2CO3) se forma quando o dióxido de carbono (CO2), também chamado de gás carbônico, se dissolve na água. Veja a reação:
H2O + CO2 - H2CO3 (ácido carbônico)
Nesse momento o pH da água pura que era 7,0 passa para 5,6, que é o equilíbrio com o CO2 atmosférico. Para a chuva ser ácida seu ph tem que ser menor que 5,6. O que faz a chuva atingir este pH é o aumento da concentração de óxidos de enxofre e óxidos de nitrogênio na atmosfera. Estes óxidos, juntamente com o óxido de carbono, são chamados de óxidos ácidos, por formarem ácidos quando em contato com a água da chuva. E assim, se forma a chamada Chuva Ácida que ao cair no ambiente terrestre, causa danos irreversíveis aos rios, lagos, matando os peixes, as plantas, etc.
A acidez da chuva no Brasil, como acontece em todo o mundo, está relacionada com o desenvolvimento urbano: cidades com maior número de fábricas, de indústrias e de veículos têm certamente, maior concentração de ácidos. E, no entanto, os ácidos causadores da chuva ácida nem sempre caem onde são produzidos, pois o vento freqüentemente carrega as nuvens para outras regiões, geralmente próximas.
Outro fator que ocasiona as chuvas ácidas, é a emissão de dióxido de enxofre (SO2) e óxido de nitrogênio pelas fábricas que usam combustíveis fósseis e usinas elétricas movidas a carvão. Esses óxidos se combinam com a umidade atmosférica gerando ácido sulfúrico (H2SO4) diluído, que é a principal precipitação atmosférica dos poluentes industriais. Veja o esquema na figura inicial.