Classificação das soluções quanto à solubilidade
A classificação das soluções quanto à solubilidade é um importante recurso utilizado em laboratórios e indústrias por estar diretamente relacionado à produção ou ao estudo de um determinado material.
Para realizar a classificação de qualquer solução quanto à solubilidade, é fundamental conhecer o coeficiente de solubilidade do soluto em relação ao solvente, presentes na mistura.
Obs.: O coeficiente de solubilidade é uma variável física que especifica a quantidade de soluto que um determinado solvente consegue dissolver, em uma dada temperatura.
A seguir, especificamos cada uma das classificações das soluções quanto à solubilidade:
Solução insaturada
Solução insaturada é aquela que apresenta uma quantidade de soluto dissolvida menor que a especificada no coeficiente de solubilidade, ou seja, ainda é possível adicionar ao solvente uma quantidade de soluto, que será dissolvida.
Por exemplo, se o coeficiente de solubilidade do NaCl em água é de 36 g a cada 100 g de H2O, a 20 oC, temos uma solução insaturada se prepararmos uma solução com 30 g de NaCl em 100 g de H2O, a 20 oC.
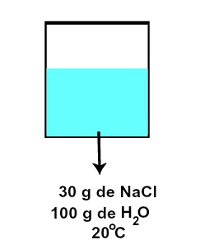
Representação de uma solução insaturada referente ao coeficiente de solubilidade
Porém, a solução insaturada pode ser classificada em diluída ou concentrada, de acordo com o seguinte critério:
-
Diluída: solução insaturada cuja quantidade de soluto dissolvida não chega nem a 50% da quantidade especificada no coeficiente de solubilidade. Assim, no caso da solução de NaCl, seria aquela preparada com 10 g de NaCl em 100 g de H2O, a 20 oC.
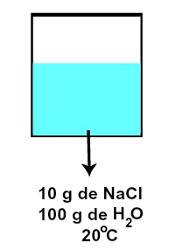
Representação da solução insaturada referente ao coeficiente de solubilidade proposto
-
Concentrada: solução insaturada cuja quantidade de soluto de soluto dissolvida é maior ou igual a 50% da quantidade especificada no coeficiente de solubilidade. Por exemplo, no caso da solução de NaCl, seria aquela preparada com 20 g de NaCl em 100 g de H2O, a 20 oC.
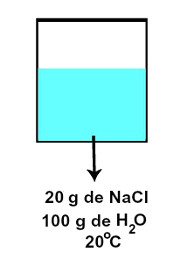
Representação da solução insaturada concentrada
Solução saturada
Solução saturada é aquela que apresenta uma quantidade de soluto dissolvida exatamente igual à especificada no coeficiente de solubilidade, ou seja, se adicionarmos ao solvente qualquer outra quantidade extra de soluto, ela não será dissolvida.
Se o coeficiente de solubilidade do NaCl em água é de 36 g a cada 100 g de H2O, a 20 oC, temos uma solução saturada se prepararmos uma solução com 36 g de NaCl em 100 g de H2O, a 20 oC.
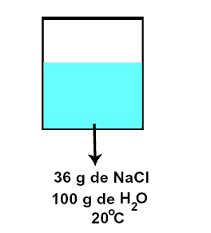
Representação da solução saturada referente ao coeficiente de solubilidade proposto
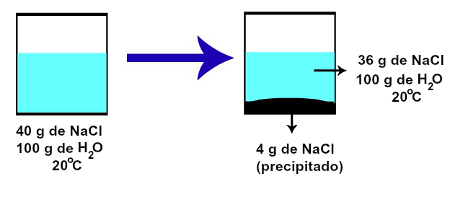
Agora, se prepararmos uma solução com 40 g de NaCl e 100 g de H2O, a 20 oC, 36g de NaCl serão dissolvidos (saturando o solvente) e os 4 g restantes serão depositados no fundo do recipiente. Por causa disso, a solução é classificada em saturada com corpo de fundo.
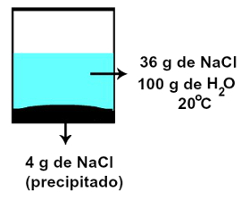
Representação da solução saturada com corpo de fundo
Solução supersaturada
Solução supersaturada é aquela que apresenta uma quantidade de soluto dissolvida superior à especificada no coeficiente de solubilidade. Para que esse tipo de solução seja formada, devemos realizar os seguintes procedimentos experimentais:
-
1o passo: Preparo de uma solução saturada com corpo de fundo (por exemplo, 40 g de NaCl em 100 g de água a 20 oC);
-
2o passo: Aquecimento da solução saturada com corpo de fundo até que todo o corpo de fundo seja dissolvido;
-
3o passo: resfriamento da solução.
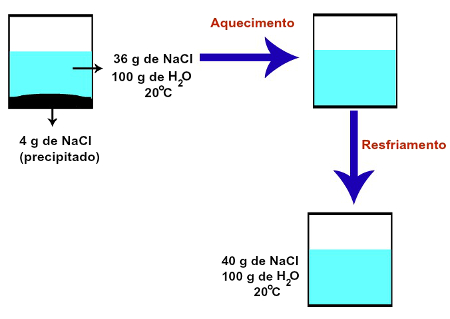
Representação da preparação de uma solução supersaturada
Após a realização desse procedimento, todo o soluto que formava o corpo de fundo passa a estar dissolvido no solvente, formando a solução supersaturada.
Caso alguma perturbação seja realizada na solução supersaturada, toda a massa de soluto dissolvida que supera o coeficiente de solubilidade passa a ser novamente corpo de fundo.