Hidratação em alcenos
Alcenos ou alquenos são hidrocarbonetos de cadeia aberta, homogênea e insaturada, na qual temos a presença de uma ligação dupla entre dois átomos de carbono. Sabe-se que a ligação dupla é composta de uma ligação sigma e uma ligação pi. A ligação sigma é uma ligação bastante estável, enquanto a ligação pi é uma ligação energeticamente mais frágil, o que favorece o seu fácil rompimento.
O fato de os alcenos ou alquenos apresentarem a ligação pi favorece as reações de adição, nas quais a ligação pi é rompida, fazendo com que seja formado um sítio de ligação em cada um dos carbonos que estavam envolvidos na ligação pi. Abaixo temos uma representação desse fato:
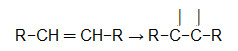
Equação geral da quebra da ligação pi de um alceno
Um exemplo das adições que os alcenos podem sofrer é a reação de hidratação. Nessa adição, o alceno sofrerá a adição dos componentes de uma molécula de água em sua estrutura. Vale ressaltar que os íons que formam uma molécula de água são o hidrônio (H+) e a hidroxila (OH-), ambos provenientes da sua autoionização. Abaixo temos a equação da autoionização da água:
.jpg)
Equação de autoionização da água
Por essa adição envolver dois íons diferentes, hidrônio e hidroxila, ela é regida pela regra de Markovnikov. De acordo com essa regra, o hidrônio será adicionado ao átomo de carbono mais hidrogenado da ligação pi rompida, enquanto o íon hidroxila será adicionado ao átomo de carbono menos hidrogenado da ligação pi rompida.
Temos a seguir a representação de uma equação de hidratação do propeno (alqueno com três átomos de carbono):
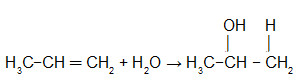
Equação de hidratação do propeno
Observação: É importante ressaltar que a hidratação de um alqueno ou alceno sempre acontece em presença de um catalisador, que é um meio ácido (preferencialmente o ácido sulfúrico, H2SO4), o que favorece a quebra da ligação pi do alceno e também a diminuição da energia de ativação que a reação necessita, fazendo com que o processo ocorra mais rápido.
A necessidade de se conhecer as reações de adição dos alquenos está relacionada com o fato de se tratar de um método de obtenção de álcoois. Assim, ao realizar uma hidratação com os alquenos é possível obter um álcool primário, um álcool secundário ou um álcool terciário. O álcool que será originado depende da posição da ligação pi no alceno, bem como o número de carbonos da cadeia. Assim:
a) Álcool primário
Para formar um álcool primário é necessário que tenhamos um alceno com apenas dois átomos de carbono. Não é possível formar um álcool primário com um alceno com mais de dois carbonos na cadeia.
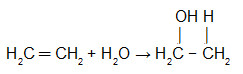
Equação que representa a hidratação do eteno
b) Álcool secundário
Para formar um álcool secundário é necessário que tenhamos um alceno de, no mínimo, três átomos de carbono. Um exemplo é a hidratação do but-2-eno:
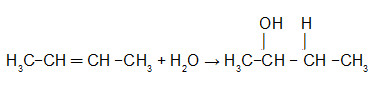
Equação que representa a hidratação do But-2-eno
c) Álcool terciário
Para formar um álcool terciário é necessário que tenhamos um alceno com mais de três átomos de carbono, porém é fundamental que a cadeia seja ramificada.
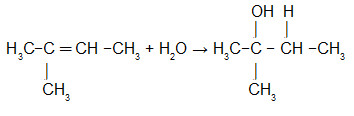
Equação que representa a hidratação do 2-metil-But-2-eno
Observação: um problema que pode ser questionado pelo estudante é: e se eu tiver na cadeia do alceno que está sendo hidratado o mesmo número de hidrogênios nos dois carbonos da dupla? Nesse caso você vai adicionar o hidrônio no carbono da ligação pi que tiver ao seu lado o maior radical e a hidroxila naquele carbono da ligação pi que tiver o menor radical.
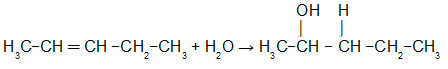
Equação que representa a hidratação do Pent-2-eno