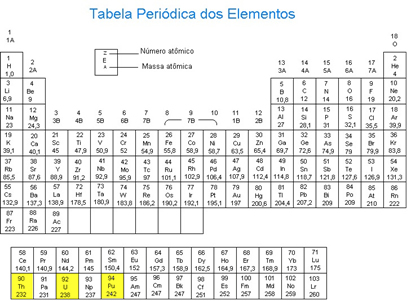
Primeira Lei de Soddy
As leis da radioatividade se referem às alterações que ocorrem no núcleo do átomo quando se emitem partículas alfa (α) ou beta (β).
O físico-químico inglês Frederick Soddy (1877-1956) foi um pioneiro no estudo da radioatividade. Ele verificou que o decaimento radioativo ocorre sempre de acordo com algumas leis básicas. Dentre elas, a primeira lei da radioatividade, conhecida como Primeira Lei de Soddy, ou simplesmente Lei de Soddy, refere-se ao decaimento radioativo pela emissão de uma partícula alfa.
Segundo essa lei, quando um átomo de um elemento emite uma partícula alfa – que é constituída de dois prótons e dois nêutrons (42α+2) – ele se transforma em outro elemento químico. Isso ocorre porque seu número atômico (Z = prótons no núcleo) diminui duas unidades e seu número de massa (A = prótons + nêutron) diminui quatro unidades.
Isso pode ser visualizado no decaimento genérico abaixo:
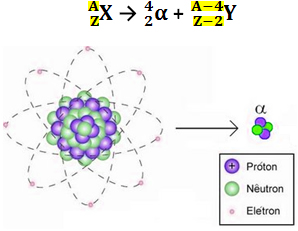
Isso significa que o átomo Y estará sempre localizado duas casas à esquerda de X na Tabela Periódica.
Veja alguns exemplos de como isso ocorre na prática:
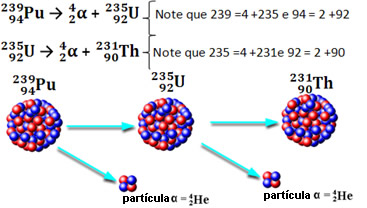
Veja a localização desses elementos na tabela periódica: