Cálculos envolvendo solubilidade
A solubilidade é um dos assuntos mais temidos dentro da Química pelos estudantes do Ensino Médio, principalmente os cálculos envolvendo a solubilidade.
Tudo isso porque esses cálculos exigem do estudante, basicamente, três pontos fundamentais:
-
Boa interpretação de texto;
-
Bom raciocínio matemático;
-
Conhecimento sobre o tema solubilidade (principalmente sobre a quantidade de soluto que está dissolvida em um solvente, a uma certa temperatura).
Com base nesses três pontos, porém, a resolução de qualquer exercício que exija os cálculos envolvendo solubilidade torna-se mais fácil.
Desta forma, o objetivo deste texto é mostrar situações em que esses cálculos estão presentes e como podem ser questionados em avaliações.
Acompanhe cada um dos seguintes exemplos:
1º Exemplo (FEI-SP): Os dados abaixo fornecem a variação do coeficiente de solubilidade (g de soluto/100 g de solvente) do nitrato de potássio em água, com a temperatura.
Dados:
20 oC ...... 32 g KNO3/100 g de H2O
80 oC .... 168 g KNO3/100 g de H2O
Resfriando-se 1340 g de solução de nitrato de potássio saturada de 80 oC até 20 oC, qual a quantidade de nitrato de potássio que se separa da solução?
Para determinar a quantidade de KNO3 que se separa da solução (cristaliza-se), devemos realizar os seguintes passos:
1º Passo: Determinar a massa de soluto presente na solução de 1340 g.
Para isso, devemos montar uma regra de três utilizando os 1340 g de solução fornecidos pelo enunciado e os 268 g (massa da solução a 80 oC, ou seja, 100 g de água e 168 g de KNO3) dados na tabela:
268 g de solução---------168 g de soluto
1340 g de H2O-------x g de soluto
268.x = 1340.168
268x = 225120
x = 225120
268
x = 840 g de soluto presentes em 1340 g de solução.
2º Passo: Determinar a massa de água presente na solução de 1340 g.
Para isso, basta subtrair da massa total da solução a massa de soluto encontrada no primeiro passo:
Massa de solvente = 1340 - 840
Massa de solvente = 500 g
3º Passo: Determinar a quantidade de soluto que os 500 g da solução fornecida pelo exercício dissolvem:
Para isso, devemos montar uma regra de três utilizando os valores do soluto e solvente fornecidos pelo exercício, a 20 oC, porque essa é a temperatura final da solução:
100 g de H2O---------32g de soluto
500 g de H2O-------x g de soluto
100.x = 500.32
100x = 16000
x = 16000
100
x = 160 g de soluto
4º Passo: Determinar a massa que será separada da solução, ou seja, que será cristalizada:
Para isso, basta subtrair da massa do soluto presente na solução (encontrada no primeiro passo) a massa do soluto que estará dissolvida na água da solução, a 20 oC, encontrada no terceiro passo:
Massa de soluto = 840 - 160
Massa de solvente = 680 g
2º Exemplo: (Unificado-RJ) A curva de solubilidade de um dado sal é apresentada abaixo.
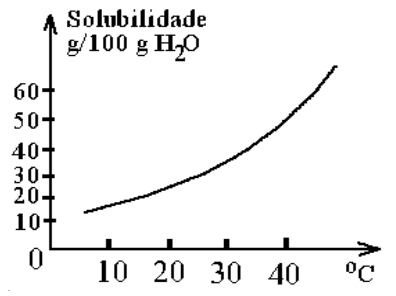
Gráfico da solubilidade do sal em água
Considerando a solubilidade deste sal a 30 ºC, qual seria a quantidade máxima (aproximada) de soluto cristalizada quando a temperatura da solução saturada (e em agitação) fosse diminuída para 20 ºC?
a) 5 g
b) 10 g
c) 15 g
d) 20 g
e) 30 g
Para determinar a quantidade de sal que se cristaliza, devemos fazer os seguintes passos:
1º Passo: Determinar a quantidade de soluto presente na solução a 30 °C.
O enunciado informa que essa solução saturada a 30 oC foi resfriada a 20 oC. Assim, se traçarmos uma reta, partindo de 30 oC até a curva e, em seguida, da curva ao eixo y (solubilidade), a massa de soluto será encontrada.
.jpg)
Determinando a massa do sal a 30 oC
Realizando a análise, em 100 g de água, é possível saber que estão dissolvidos aproximadamente 35 g de sal.
2º Passo: Determinar a massa de sal dissolvida em 100 g de H2O a 20 oC.
Nesse passo, devemos realizar o mesmo procedimento feito no primeiro passo, mas considerando-se a 20 oC.
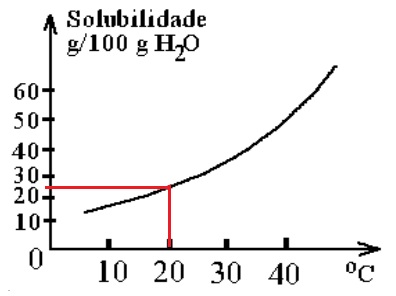
Determinando a massa do sal a 20 oC
Logo, com a análise, temos que a 20 oC, 100 g de H2O dissolvem aproximadamente 25 g de sal.
3º Passo: Determinar a massa que será cristalizada.
Para determinar a massa de sal que será cristalizada, basta subtrair da massa do soluto que estava dissolvida na solução a 30 oC (1º passo) a massa do soluto que está dissolvida a 20 oC (2º passo):
Massa cristalizada = 35 - 25
Massa cristalizada = 10 g de sal cristalizado
3º Exemplo 3- (Unesp-SP) A quantidade máxima de soluto que pode ser dissolvida numa quantidade padrão de solvente é denominada Coeficiente de Solubilidade. Os valores dos Coeficientes de Solubilidade (g de KNO3 por 100 g de H2O) do nitrato de potássio (KNO3) em função da temperatura são mostrados na tabela.
.jpg)
Tabela contendo o coeficiente de solubilidade do KNO3
Considerando-se os dados disponíveis na tabela, a quantidade mínima de água (H2O), a 30 ºC, necessária para dissolver totalmente 6,87 g de KNO3, será de:
a) 15 g.
b) 10 g.
c) 7,5 g.
d) 3 g.
e) 1,5 g.
Para determinar a massa de H2O mínima necessária para dissolver 6,87 g de soluto, basta montar uma regra de três utilizando o conhecimento (retirado da tabela) de que 100 g de H2O dissolvem 45,8 g de soluto, a 30 oC:
100 g de H2O---------45,8 g de soluto
x g de H2O-------6,87 g de soluto
45,8.x = 100.6,87
45,8x = 687
x = 687
45,8
x = 15 g de H2O
4º Exemplo- (UEL-PR) Uma solução saturada de cloreto de ouro de massa igual a 25,20 gramas foi evaporada até a secura, deixando um depósito de 10,20 gramas de cloreto de ouro. A solubilidade do cloreto de ouro, em gramas do soluto por 100 gramas do solvente, é:
a) 10,20
b) 15,00
c) 25,20
d) 30,35
e) 68,00
Para determinar a quantidade de soluto que pode ser dissolvida em 100 g de H2O, devemos fazer os seguintes passos:
1º Passo: Determinar a massa de solvente evaporada.
Para isso, basta subtrair da massa total da solução a massa de soluto restante:
Massa de solvente evaporada = 25,2 g – 10,2 g
Massa de solvente evaporada = 15 g
2º Passo: Determinar a massa de soluto que pode ser dissolvida em 100 g de H2O.
Para isso, basta montar uma regra de três utilizando o conhecimento de que 15 g de H2O dissolvem 10,2 g de soluto, conforme o que foi obtido no primeiro passo:
15 g de H2O---------10,2 g de soluto
100 g de H2O-------x g de soluto
15.x = 100.10,2
15x = 1020
x = 1020
15
x = 68 g de soluto