Oxidação branda em alcinos
A reação de oxidação é aquela em que temos o aumento do nox de uma espécie química, mas ela sempre vem acompanhada de uma redução, reação na qual ocorre a diminuição do nox de uma espécie. Quando esse tipo de reação ocorre com compostos orgânicos, o elemento químico que sofrerá oxidação sempre será o carbono.
Como as reações de oxidação envolvem redução e oxidação, temos a presença de um reagente redutor (aquele que sofre oxidação) e um reagente oxidante (aquele que sofre redução). A oxidação ocorre no composto orgânico e a redução acontece no outro reagente envolvido na reação.
Existem quatro tipos de oxidação: combustão, branda, energética e ozonólise. Daremos ênfase neste texto à oxidação branda que ocorre em alcinos (hidrocarboneto insaturado que apresenta uma ligação tripla entre dois carbonos).
A oxidação branda é uma reação orgânica que ocorre somente em hidrocarbonetos insaturados (presença de dupla ligação ou tripla ligação). O agente oxidante utilizado nela é o chamado reagente de Bayer (permanganato de potássio) em presença de água e uma base inorgânica (XOH, que libera OH- em água).
Quando o reagente de Bayer está em meio aquoso e básico, ele produz dois óxidos (óxido de potássio-K2O e dióxido de manganês-MnO2) e oxigênios nascentes ([O]).
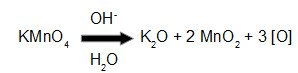
Equação da reação do reagente de Bayer em meio básico
Os alcinos apresentam na sua constituição duas ligações pi entre dois átomos de carbono. Na oxidação branda, as duas ligações são rompidas, gerando assim dois sítios de ligação em cada um dos átomos de carbono que realizavam a ligação pi. Veja a representação dessa quebra:
.jpg)
Representação do rompimento das ligações pi de um alcino
São os oxigênios nascentes provenientes do reagente de Bayer, associados a um átomo de hidrogênio (grupos OH), que promovem o ataque aos sítios de ligação criados quando as duas ligações pi presentes no alcino foram rompidas. Acompanhe a representação a seguir:
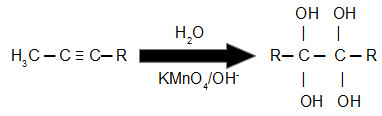
Equação geral de um alcino reagindo com reagente de Bayer
Quando os grupos OH atacam os sítios de ligação, podemos observar duas hidroxilas ligadas a um mesmo átomo de carbono. Esse agrupamento de átomo é denominado de diálcool gêmino, ou seja, duas hidroxilas em um átomo de carbono saturado. Como são dois carbonos apresentando essa característica, dizemos que a reação de um alcino com o reagente de Bayer em meio básico forma um diol-gêmino vicinal, pois esses carbonos estão um ao lado do outro.
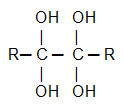
Fórmula geral de um diálcool-gêmino vicinal
Os dióis-gêminos são estruturas extremamente instáveis e, após sua formação, sofrem uma desidratação imediata. Em cada diol-gêmino, temos duas hidroxilas (OH); por isso, uma delas interage com o hidrogênio da outra, formando uma molécula de água. O oxigênio que sobra dessas duas hidroxilas passa a realizar uma ligação dupla com o carbono.
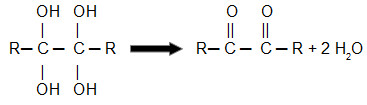
Equação geral de desidratação de um diol-gêmino vicinal
A oxidação branda de um alcino resulta sempre em um composto final que apresenta dois grupos funcionais iguais ou diferentes. O tipo de grupo funcional depende do tipo de carbono ligado à tripla ligação. Podemos ter na ligação tripla dois carbonos primários, um primário e um secundário ou dois secundários. A seguir temos equações que representam todas essas situações, porém, se:
-
o carbono for primário, formará um aldeído;
-
o carbono for secundário, formará uma cetona.
1º Exemplo: alcino com carbonos primários na tripla
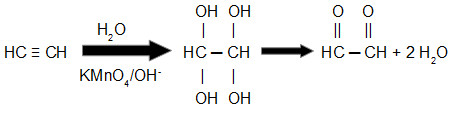
Equação de oxidação branda do etino
Nesse exemplo, podemos observar que o produto final apresenta dois grupos aldeídos.
2º Exemplo: alcino com um carbono primário e outro secundário na tripla
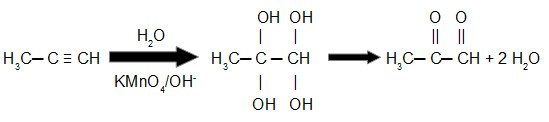
Equação de oxidação branda do propino
Nesse exemplo podemos observar que o produto final apresenta um grupo aldeído e um grupo cetona.
3º Exemplo: alcino com carbonos secundários na tripla
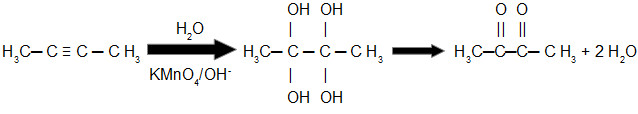
Equação de oxidação branda do but-2-ino
Nesse exemplo podemos observar que o produto final apresenta dois grupos cetona.

