Aldeídos e cetonas
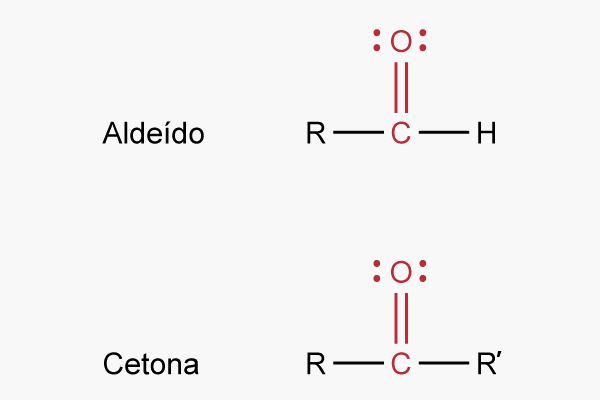
Aldeídos e cetonas são funções orgânicas oxigenadas que têm em comum a presença do grupo carbonila, C=O. Contudo, enquanto os aldeídos têm a carbonila na extremidade da cadeia, as cetonas apresentam essa carbonila sempre entre dois átomos de carbono. Além disso, recomenda-se, segundo a Iupac, que aldeídos recebam o sufixo −al e que cetonas recebam o sufixo −ona.
Aldeídos e cetonas são suscetíveis à ataques nucleofílicos, mais especificamente reações de adição nucleofílica. Isso é consequência da maior carga parcial positiva do carbono da carbonila, em consequência da alta eletronegatividade do oxigênio. Para essas reações, aliás, percebe-se uma maior reatividade por parte do aldeído do que da cetona.
Leia também: Como identificar as funções orgânicas?
Resumo sobre aldeídos e cetonas
- Aldeídos e cetonas são funções orgânicas oxigenadas que têm em comum a presença do grupo carbonila.
- Os aldeídos têm a carbonila na extremidade da cadeia.
- As cetonas têm a carbonila entre dois carbonos.
- Aldeídos, segundo a Iupac, têm sufixo –al.
- Cetonas têm sufixo –ona.
- Aldeídos e cetonas, por conta da maior carga parcial positiva do carbono da carbonila, são suscetíveis à ataques nucleofílicos e, assim sendo, sofrem adições nucleofílicas.
O que são aldeídos e cetonas?
Aldeídos e cetonas são funções orgânicas oxigenadas que têm em comum a presença do grupo carbonila (C=O). No caso dos aldeídos, a carbonila se localiza na extremidade da cadeia, sendo que uma das ligações do carbono nela é com um átomo de hidrogênio, enquanto a outra é com uma cadeia carbônica qualquer (com exceção do formaldeído, em que a carbonila se liga a dois átomos de hidrogênio).
Já as cetonas são muito semelhantes em relação aos aldeídos, com a diferença de que a carbonila está ligada a dois átomos de carbono. Assim sendo, a carbonila da cetona nunca se localiza na extremidade da cadeia.
Como diferenciar aldeído de cetona?
Embora sejam muito semelhantes estruturalmente, aldeídos e cetonas têm particularidades que devem ser levadas em consideração. A principal delas é a posição da carbonila.
Enquanto nos aldeídos a carbonila se localiza na extremidade da cadeia (sendo obrigatoriamente identificada como o carbono de número 1), nas cetonas a carbonila deve estar obrigatoriamente ligada a dois carbonos, o que quer dizer que essa carbonila nunca será o carbono da extremidade da cadeia.
Tal particularidade traz algumas consequências estruturais para aldeídos e cetonas. Por exemplo, não é possível criar aldeídos de cadeia fechada, enquanto é possível cadeias fechadas de cetonas (como é o caso das quinonas).
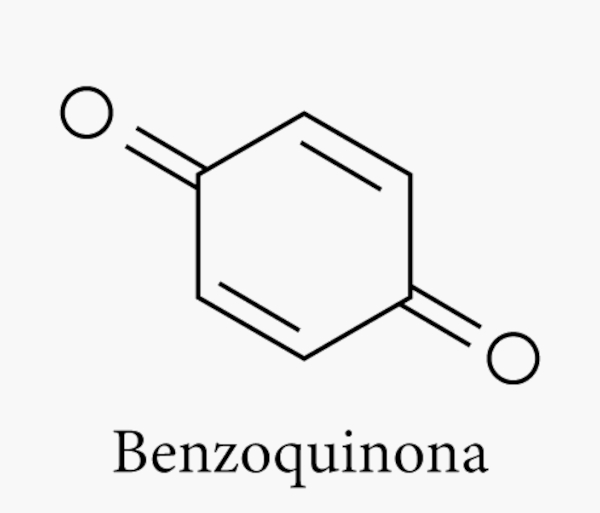
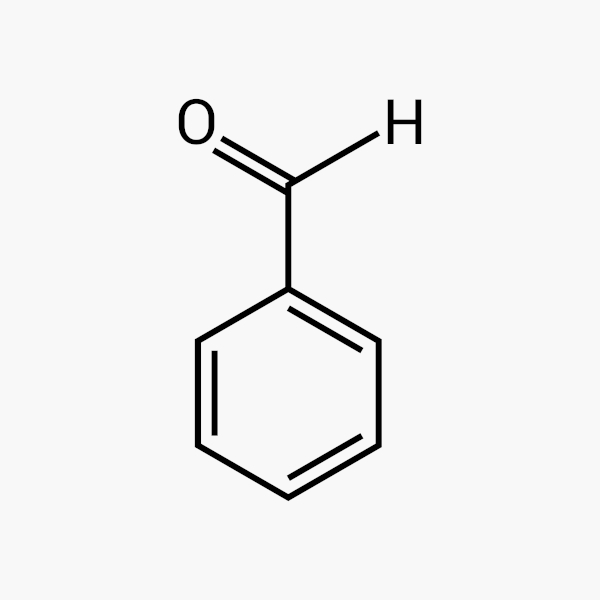
Isso não quer dizer que não existem estruturas fechadas em cadeias de aldeídos, como é o caso do fenilmetanal (benzaldeído). Contudo, como é possível perceber, a carbonila não se liga a um carbono da cadeia fechada, mas sim se comporta como um carbono da cadeia aberta.
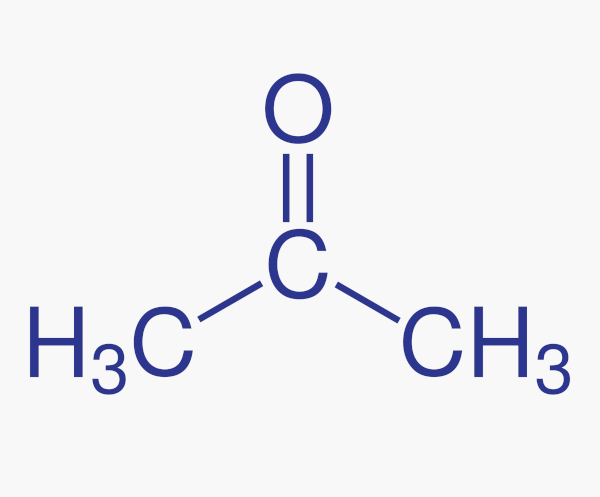
Outro ponto de interesse é que não existem cetonas com menos de três carbonos, pois, contando com o carbono da carbonila, são necessários, no mínimo, três carbonos para configurar uma cetona. Diferentemente dos aldeídos, em que é possível fazer cadeias mesmo com um carbono (é o caso do formaldeído, metanal).
Nomenclatura de aldeídos e cetonas
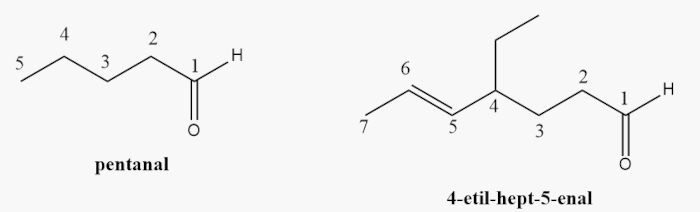
Segundo a União Internacional de Química Pura e Aplicada, os aldeídos têm sufixo −al, enquanto as cetonas têm sufixo −ona. No caso do aldeído, o grupo funcional é sempre o carbono de número 1 e, portanto, não precisa ser nomeado. Veja alguns exemplos.
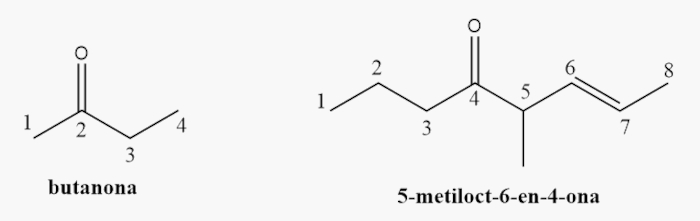
Já nas cetonas, a carbonila pode adotar posições diferentes e, portanto, deve ser numerada. No entanto, como estabelece a Iupac, os grupos funcionais devem ter o menor número possível. A exceção dessa regra fica para as cetonas de 3 e 4 carbonos, cuja posição da carbonila é sempre a mesma, independentemente da forma como é desenhada, e, neste caso, a posição deve ser omitida na nomenclatura oficial.
Reações de aldeídos e cetonas
Tamanha semelhança em aldeídos e cetonas permite que ambos tenham reações semelhantes. Isso porque, em ambos os casos, a carbonila é suscetível a ataques nucleofílicos, uma vez que o carbono apresenta relativa carga parcial positiva, em decorrência da grande eletronegatividade do átomo de oxigênio, o qual atrai para si a densidade eletrônica da ligação C=O.
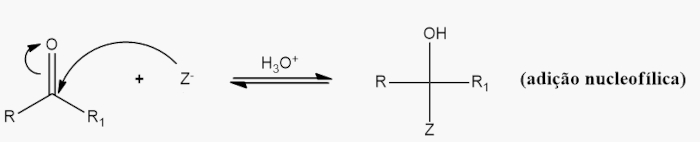
Dessas reações nucleofílicas, podemos pensar que, inicialmente, dois mecanismos são possíveis: uma substituição ou uma adição. Entretanto, a substituição nucleofílica não é viável para aldeídos e cetonas, pois, por essa rota, haveria a formação das bases de Lewis H− ou R−, as quais são muito fortes e reativas, não se estabilizando no meio reacional. Com isso, resta apenas a adição nucleofílica, conforme esquema geral a seguir.
Em termos de reatividade, os aldeídos são, em geral, mais reativos que a cetona. Isso porque as cadeias carbônicas apresentam um maior efeito indutivo doador de elétrons em comparação ao hidrogênio. Como consequência, a carga parcial positiva da carbonila de cetona é um pouco menor e, assim sendo, menos atrativa para ataques nucleofílicos quando comparada a aldeídos.
Outro ponto que diminui a reatividade das cetonas em comparação aos aldeídos é o chamado efeito estérico. As cadeias carbônicas são mais volumosas que o átomo de hidrogênio, o que dificulta, em termos espaciais, o ataque por parte do nucleófilo.
O meio ácido na reação de adição nucleofílica é necessário para se fazer a protonação do átomo de oxigênio, o qual tem pares de elétrons não ligantes (disponíveis). Essa protonação aumenta, ainda mais, a carga parcial positiva do carbono da carbonila.
Seguem alguns exemplos de adições nucleofílicas:
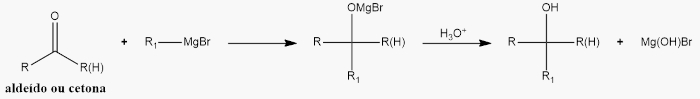
- Reações com compostos organometálicos (Grignard):
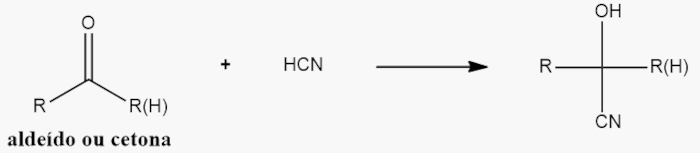
- Reações com cianeto:
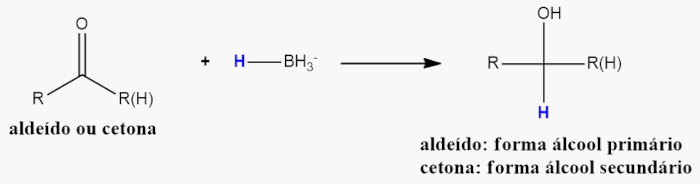
- Reações com hidretos:
Saiba mais: Álcoois — função orgânica caracterizada pela presença do grupo hidroxila (-OH)
Exercícios resolvidos sobre aldeídos e cetonas
Questão 1. (USS Univassouras Medicina/2023.2) A substância representada pela fórmula estrutural a seguir é um dos principais componentes do óleo obtido da citronela.
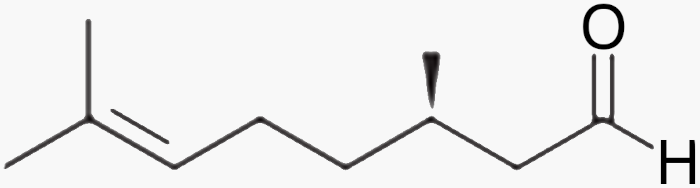
Esse composto pertence à função orgânica denominada:
(A) éter.
(B) álcool.
(C) cetona.
(D) aldeído.
Resposta: Letra D.
Percebe-se na substância representada a função carbonila na extremidade da cadeia, ligada a um átomo de hidrogênio, o que caracteriza a função aldeído.
Questão 2. (FCM PB Medicina/2021.1) Nas últimas décadas tem-se observado um grande aumento no interesse pelo potencial terapêutico das plantas medicinais e aromáticas. Os óleos essenciais são misturas complexas de compostos voláteis produzidos pelas plantas e isolados somente por processos físicos. Entre as propriedades farmacológicas, descritas na literatura para esses óleos essenciais, destacam-se os efeitos repelente, anti-inflamatório, antiasmático, ansiolítico e anticâncer. Para cada flor, uma combinação específica de óleos essenciais que determina o aroma característico. A seguir, estão apresentadas algumas substâncias orgânicas presentes no aroma de algumas flores comuns e que apresentam um elevado efeito farmacológico.
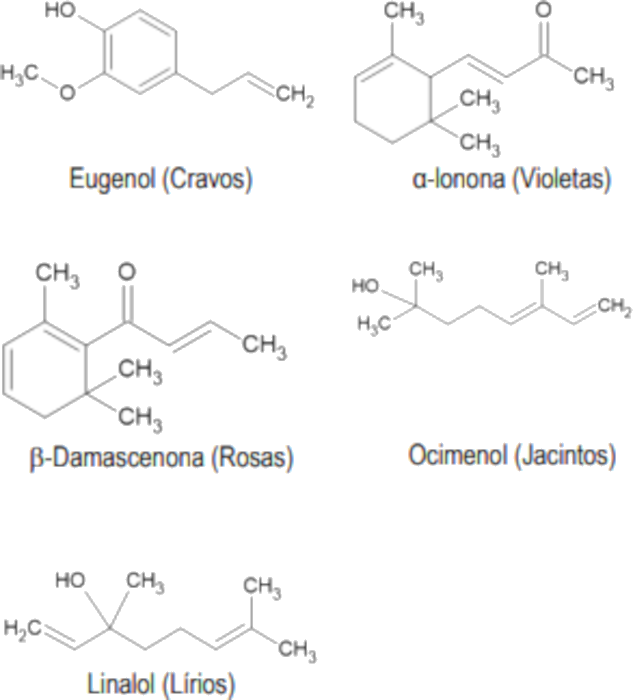
A função cetona está presente nas substâncias que compõem o aroma de:
(A) Cravos e lírios.
(B) Jacintos e cravos.
(C) Violetas e rosas.
(D) Rosas e lírios.
(E) Violetas e jacintos.
Resposta: Letra C.
O grupo funcional carbonila (C=O) entre dois átomos de carbono só é percebido em duas estruturas: beta-damascenona (rosas) e alfa-lonona (violetas).
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
INTERNATIONAL UNION OF PURE AND APPLIED CHEMISTRY – IUPAC. Glossary of terms used in physical organic chemistry. Pure and Applied Chemistry, Reino Unido, 1994.
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volumes 1 e 2. 12. ed. Rio de Janeiro: LTC, 2018.