Emulsão
Emulsão é uma dispersão coloidal em que gotas de um líquido são dispersas em uma outra fase líquida contínua, de composição química diferente. Tais líquidos, aliás, são imiscíveis. As emulsões, na maioria das vezes, apresentam um aspecto leitoso, com certa opacidade. São aplicadas em diversos setores da indústira, como na de alimentos e farmacêutica.
A emulsão é termodinamicamente instável, o que quer dizer que não se mantém por muito tempo após se formar. Sua estabilidade é garantida pela ação de emulsificantes, substâncias de caráter anfifílico que impedem a reaglutinação das gotas dispersas.
Leia também: Quais são os tipos de dispersões?
Resumo sobre emulsão
-
Emulsões são dispersões coloidais, em que um líquido, na forma de gotas, está disperso em outro, de composição química diferente.
-
Tais líquidos são imiscíveis, sendo um aquoso (de maior caráter polar) e sendo o outro um composto orgânico (de menor caráter polar).
-
Boa parte das emulsões possuem um aspecto leitoso, embora outras aparências sejam possíveis.
-
As emulsões são termodinamicamente instáveis.
-
Os emulsificantes são agentes utilizados para estabilizar emulsões, evitando que as mesmas se desfaçam.
-
As emulsões são aplicadas em diversos setores da indústria, como na de alimentos, de tintas, de cosméticos e cuidado pessoal, entre outros setores de grande importância econômica.
O que é emulsão?
Emulsão é uma dispersão coloidal em que um líquido, na forma de gotas, é disperso em uma fase líquida contínua de composição diferente. A fase que está dispersa é, por vezes, conhecida como fase interna, enquanto a fase contínua é conhecida como fase externa:

Características da emulsão
Nem todas as emulsões possuem o aspecto leitoso clássico, com certa opacidade. Na verdade, há uma grande variedade de aparências, que dependem do tamanho das gotas dispersas e dos índices de refração entre os meios. Por exemplo, uma emulsão pode ser transparente se os dois meios possuírem o mesmo índice de refração ou ainda se as gotas dispersas forem muito pequenas comparadas ao comprimento de onda da luz usada para iluminação.
A textura das emulsões irá depender da fase líquida contínua usada como dispersante. Emulsões em que uma solução aquosa é usada como dispersante terão um aspecto mais aquoso ou cremoso, enquanto as que possuem líquidos orgânicos (óleos) terão um aspecto mais oleoso. Claro que a viscosidade também impacta na textura final, então mesmo uma emulsão em solução aquosa poderá ter aspecto oleoso se o líquido tiver uma alta viscosidade.
De modo geral, as emulsões também não são termodinamicamente estáveis, embora na prática algumas emulsões possam resistir por semanas, meses e até mesmo anos. Nesse contexto, adiciona-se um emulsificante, que atua como uma camada protetora das gotas dispersas, de modo a aumentar sua estabilidade. Nesse contexto, deve-se dizer que a formação de uma emulsão requer absorção de energia, sendo caracterizada como um processo não espontâneo.
Importante: No conceito de dispersão coloidal, entende-se que as partículas, gotas ou bolhas dispersas na outra fase devem ter tamanho entre 1 e 1000 nm (nanômetros, 10−9 m). Contudo, em emulsões na prática pode ocorrer de as gotas dispersas superarem os limites de tamanho de uma dispersão coloidal, chegando à escala de dezenas ou até mesmo centenas de micrômetros (10−6 m).
Veja também: Aerossol — dispersão coloidal que possui características intermediárias entre os compostos homogêneos e heterogêneos
Tipos de emulsão
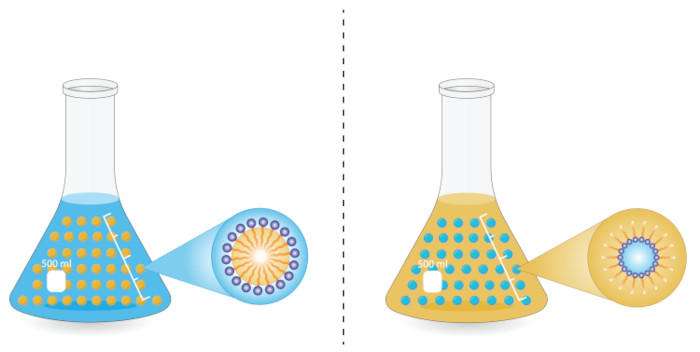
Na maioria das emulsões, um dos líquidos é aquoso, enquanto o outro é comumente um líquido orgânico, referido como óleo (dada sua hidrofobicidade). Por isso, emulsões são identificadas pelas letras W (do inglês water, que significa água) e O (do inglês oil, que significa óleo). Assim, podemos identificar, rapidamente, duas emulsões:
-
W/O: “water-in-oil” (água-no-óleo), que significa gotas de água dispersas no líquido orgânico.
-
O/W: “oil-in-water” (óleo-na-água), que significa gotas de óleo dispersas no líquido aquoso.
-
O/O: “oil-in-oil” (óleo-no-óleo), que significa que gotas de óleo (dessa vez, um líquido orgânico de caráter polar) dispersas no líquido orgânico.
Mesmo assim, na prática as emulsões podem se apresentar de forma mais complexa, sendo que, por exemplo, pode haver uma emulsão na emulsão (emulsões duplas), classificadas como O/W/O (em que gotas do líquido orgânico estão dispersas em gotas de água que estão dispersas em uma fase líquida orgânica contínua) e W/O/W (o inverso da O/W/O).
Como funciona uma emulsão?
Uma emulsão é um tipo de dispersão coloidal, em que um líquido, na forma de gotas, está disperso em outro. Sendo assim, pode-se formar uma emulsão colocando os dois líquidos em um recipiente, agitando-o posteriormente.
Ocorre que os líquidos formadores da emulsão são imiscíveis, e, além disso, as emulsões são sistemas termodinamicamente instáveis. Assim sendo, após a agitação, espera-se que essa emulsão simplesmente se desfaça pouco tempo depois. Por isso, um emulsificante deve ser adicionado, de modo a proporcionar miscibilidade e aumentar a estabilidade da emulsão.
Espera-se que o emulsificante diminua a tensão interfacial (entre as fases) da emulsão, fazendo com que se formem gotas menores mais facilmente e mais estáveis, de modo que elas não se reagrupem em gotas maiores e terminem com a emulsão (um efeito conhecido como coalescência) ou até mesmo que não haja separação entre as fases.
De toda forma, emulsões com gotas maiores (na faixa de alguns micrômetros) são mais fáceis de serem produzidas que as com gotas menores (na faixa de nanômetros), as quais necessitam de grande energia e maior quantidade de surfactante. Uma emulsão estável deve apresentar aspecto homogêneo, porém uma mínima separação entre fases é ainda aceitável.
Agentes emulsificantes
Emulsificantes compõem um grupo de compostos orgânicos que possuem dois grupos distintos: um solúvel em água (hidrofílico) e outro insolúvel ou muito pouco solúvel em água (hidrofóbico). Os emulsificantes facilitam a formação da emulsão e/ou aumentam a estabilidade coloidal ao diminuírem os índices de agregação entre as gotas e também a coalescência entre estas.
Os emulsificantes criam uma barreira em volta das gotas, diminuindo a tensão interfacial. Também é possível que os emulsificantes criem cargas nas gotas da emulsão, diminuindo o contato físico entre elas e, assim, diminuindo a probabilidade de coalescência.
Na imagem abaixo, temos ao centro um recipiente com água no qual estão sendo colocadas gotas de óleo. À esquerda desse recipiente, temos um recipiente no qual não foi usado emulsificante, sendo possível ver que a água e o óleo não se misturam e estão bastante divididos. À direita desse recipiente, temos um recipiente no qual foi usado emulsificante, por isso temos uma emulsão.
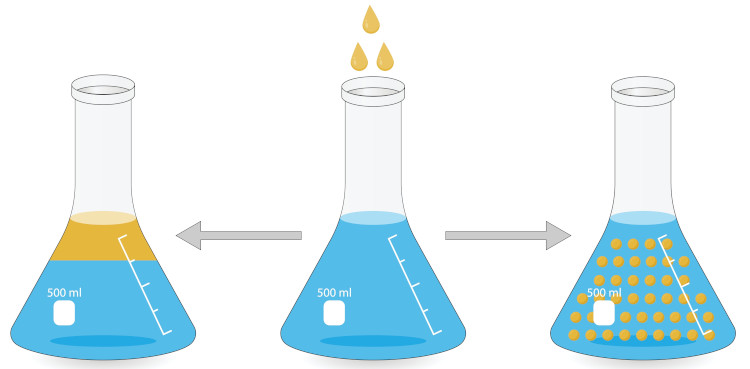
Além disso, tais substâncias devem ser inertes em relação à emulsão, não reagindo com ela, além de quimicamente estáveis e atóxicas. Espera-se que também sejam inodoras, não causem irritação e sejam baratas. Entre os principais emulsificantes estão o lauril sulfato de sódio, o dioctil sulfosuccinato de sódio (docusato de sódio), além dos polímeros conhecidos como Span e Tween.
Os emulsificantes podem ser divididos de acordo com sua estrutura química:
-
Sintéticos: aniônicos, catiônicos, não iônicos e anfotéricos.
-
Naturais: derivados vegetais, derivados animais, agentes semissintéticos, agentes sintéticos.
-
Sólidos finamente dispersos: bentonita.
-
Auxiliares: ácidos graxos, álcoois graxos e ésteres de ácidos graxos.
Importante: Para emulsificantes, também se desenvolveu um sistema conhecido como HLB (balanço hidrofílico-lipofílico), que auxilia na tomada de decisão acerca da quantidade e do tipo de emulsificante a ser utilizado. Os valores de HLB são determinados experimentalmente, podendo variar entre 1 e 18. Um emulsificante com HLB baixo indica que ele possui baixo índice de grupos hidrofílicos e alto índice de grupos lipofílicos. Já um emulsificante com o HLB alto indica o contrário: alto índice de grupos hidrofílicos e baixo índice de grupos lipofílicos.
Emulsão no cotidiano

As emulsões são aplicadas em diversos setores de interesse da indústria. Os principais são:
-
Alimentos: maionese, cremes para saladas, sobremesas, bebidas.
-
Cosméticos e cuidado pessoal: cremes para as mãos, loções, protetores solares, sprays para cabelo.
-
Farmacêutica: anestésicos, emulsões lipídicas, emulsões duplas e múltiplas.
-
Tintas: emulsões de resinas alquídicas ou emulsões de látex.
Outros produtos de emulsão são inseticidas e herbicidas, produtos para polimento, pavimentação de asfalto e isolantes térmicos e elétricos. Do ponto de vista ambiental, emulsões também são utilizadas no tratamento de águas e esgotos (na floculação e coagulação) e na remediação de solos.
Fontes
IUPAC. Glossary of terms used in physical organic chemistry. Pure and Applied Chemistry, Reino Unido, v. 66, n. 5, p. 1077-1184, 1994.
SCHRAMM, L. L. Emulsions, Foams and Suspensions: Fundamentals and Applications. Weinheim, Alemanha: Wiley-VCH, 2005.
SARATHCHANDRAPRAKASH, N. K.; CHANDRIKAMAHENDRA, S. J.; PRASHANTH, K. M.; BABU, U. V.; GOWDA, D. V. S. Emulsions and emulsifiers. The Asian Journal of Experimental Chemistry, v. 8., n. 1 e 2, p. 30-45, Jun e Dez. 2013.
TADROS, T. F. Emulsion Science and Technology. Weinheim, Alemanha: Wiley-VCH, 2009.


