Explicação de Dalton para as Leis Ponderais
No ano de 1803, o químico inglês John Dalton (1766-1844) desenvolveu uma teoria sobre a estrutura da matéria, retomando a ideia dos filósofos Demócrito e Leucipo. Ele estabeleceu uma teoria que pode ser vista com mais detalhes no texto “Teoria atômica de Dalton”, mas resumidamente seus postulados eram:
1. Toda matéria é formada de minúsculas partículas esféricas e maciças denominadas átomos, que não podem ser criados nem destruídos. Cada substância é constituída de um único tipo de átomo;
2. Os elementos são formados por átomos isolados iguais, com mesma massa e tamanho, sendo eles indivisíveis;
3. A combinação de diferentes átomos numa proporção de números inteiros origina substâncias diferentes.
Os postulados de Dalton puderam, então, explicar as leis ponderais de Antoine Lavoisier e Joseph Louis Proust.
Conforme explanado no texto “Lei de Lavoisier”, esse cientista, por meio de fatos experimentais, elaborou a Lei de Conservação das Massas, que atualmente é conhecida pelo seguinte enunciado:
“Na natureza, nada se perde, na se cria, tudo se transforma.”
Isso significa que em uma reação que ocorra em sistema fechado, a massa total dos regentes é sempre igual a massa total dos produtos, quaisquer que sejam as transformações que venham a ocorrer. Dalton, por sua vez, propôs que a matéria é formada por átomos que não podem ser criados nem destruídos. Isso leva à seguinte conclusão lógica: se o número de átomos permanece constante durante uma reação, então a massa do sistema também se manterá constante.
Por exemplo, usando o modelo de átomos esféricos de Dalton, veja uma reação em que se verifica que 3g de carbono reagem com 8g de oxigênio, produzindo 11 g de gás carbônico:
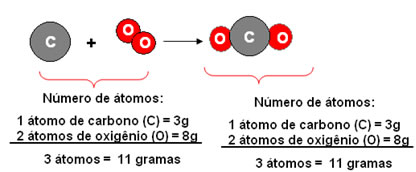
Veja que o que ocorre é, conforme Dalton disse, um rearranjo dos átomos, em combinações diferentes originando substâncias diferentes.
Já a Lei das Proporções Constantes, vista no texto “Lei de Proust”, diz:
“Toda substância apresenta uma proporção em massa constante na sua composição.”
A teoria de Dalton também explicou essa lei em nível microscópico. No mesmo exemplo citado anteriormente da reação de formação do gás carbônico, vimos que:
3 g de carbono (C) se unem a 8 g de oxigênio (O2) produzindo 11 g de gás carbônico (CO2).
Se desejarmos obter duas moléculas de CO2 deveremos usar o dobro das quantidades, tanto de carbono como de oxigênio:
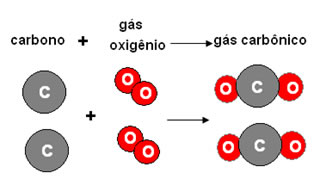
Como a proporção em número de átomos é constante, a proporção em massa também é constante. Qualquer que seja a experiência para a obtenção do gás carbônico, a proporção entre os átomos de carbono e oxigênio se mantém constante.

