Inibidores e venenos de catalisador
Os catalisadores são substâncias que aumentam a velocidade média de determinadas reações por alternar o mecanismo delas, provendo barreiras energéticas menores para a formação do complexo ativado sem serem consumidos na reação em que participam.
Assim, em muitas indústrias, os catalisadores são usados para acelerar reações que demorariam muito para formar pouca quantidade de produto. No entanto, pode acontecer do catalisador não funcionar como se gostaria, ocasionando problemas na produção. Geralmente, isso acontece em virtude da presença de substâncias denominadas de anticatalisadores, inibidores de catalisador ou, ainda, de veneno de catalisador.
Tais compostos realizam a inibição catalítica, ou seja, têm a propriedade de inibir ou anular a ação dos catalisadores na reação.
Por exemplo, o arsênio é um veneno de catalisador. Na produção da amônia (NH3), usa-se um processo conhecido como Haber-Bosch, que usa o ferro como catalisador. Também na combustão do SO2(g) para a produção do trióxido de enxofre (SO3(g)) usa-se a platina metálica (Pt(s)) como catalisadora. No entanto, se houver arsênio (As(s)) como impureza no meio desses dois processos, a ação catalítica da platina e do ferro é inibida.

No caso da produção da amônia, infelizmente não há outro catalisador que seja vantajoso como o ferro. Mas, no caso da combustão do SO2(g), pode-se usar o pentóxido de divanádio (V2O5(s)) como catalisador no lugar da platina, pois ele é bem mais resistente à ação de anticatalisadores.
Agora, existem também substâncias que são chamadas apenas de “inibidores”, que são aquelas que têm um efeito contrário ao dos catalisadores, ou seja, diminuem a velocidade das reações, porque possuem a propriedade de aumentar a energia de ativação necessária para que os reagentes consigam formar o complexo ativado.
Nas indústrias, os inibidores são usados quando se quer, por exemplo, calcular a velocidade de reações muito rápidas ou, então, quando se deseja retardar determinadas reações.
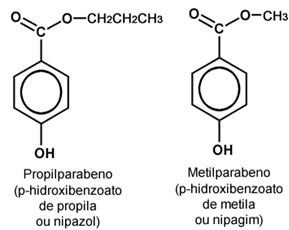
Por exemplo, a decomposição de alimentos, bebidas, cosméticos, remédios e de outros produtos são reações que se deseja que ocorram o mais lentamente possível. Por isso, são adicionados conservantes, que são inibidores, tais como os parabenos, cujas estruturas são mostradas abaixo: