Reações com óxidos anfóteros
As reações com óxidos anfóteros ocorrem quando as substâncias dessa classe dos óxidos (as outras classes são os óxidos ácidos, básicos e duplos) são colocadas em um mesmo meio que um ácido ou uma base. Lembrando que os óxidos anfóteros são aqueles formados pelos elementos zinco, alumínio, cromo (de NOX +3) e estanho.
Uma reação química ocorre quando o óxido anfótero interage com ácido ou base porque esses óxidos apresentam característica dual, ou seja, podem atuar como um composto de caráter ácido ou básico. Assim:
-
Óxido anfótero com base – o óxido atua como um ácido;
-
Óxido anfótero com um ácido – o óxido atua como uma base.
Por causa de todas essas características, as reações entre óxidos anfóteros e ácido ou base são reações de neutralização, que formam obrigatoriamente um sal e água:
Óxido anfótero + ácido → sal + água
ou
Óxido anfótero + base → sal + água
Reação de óxido anfótero com ácido
Quando um óxido anfótero reage com um ácido, o cátion metálico (Y+) do óxido interage com o ânion (X-) do ácido para formar o sal (YX), e o cátion hidrônio (H+) do ácido interage com o ânion do óxido (O-2):
YO + HX → YX + H2O
Exemplo: reação entre o óxido de cromo III (Cr2O3) e o ácido sulfúrico (H2SO4)
Cr2O3 + H2SO4 →
O óxido de cromo III apresenta os íons cromo III (Cr+3) e óxido (O-2), os quais interagem, respectivamente, com os íons sulfato (SO4-2) e hidrônio (H+) do ácido, formando os compostos sulfato de cromo III [Cr2(SO4)3] e água (H2O). Veja a seguir a equação balanceada desse processo:
Cr2O3 + 3 H2SO4 → Cr2(SO4)3 + 3 H2O
Reação de óxido anfótero com base
Quando um óxido anfótero reage com uma base, o cátion metálico (Y+) da base interage com o ânion (YO-) formado a partir do metal presente no óxido para formar o sal (WYO), e o hidrônio (H+), que sobra do hidróxido (OH-) da base, interage com o ânion do óxido (O-2), formando a molécula de água.
O ânion formado a partir do metal presente no óxido resulta da interação com o oxigênio da hidroxila da base:
YO + WOH → WYO + H2O
A tabela abaixo mostra os possíveis ânions formados pelos metais que compõem um óxido anfótero:
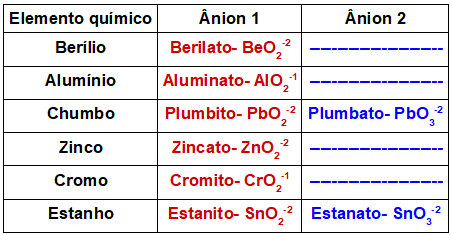
Tabela de ânions contendo metais
Exemplo: Reação entre o óxido de alumínio e o hidróxido de cálcio.
Al2O3 + Ca(OH)2 →
O óxido de alumínio apresenta os íons alumínio (Al+3), que forma o ânion aluminato (AlO2-), e óxido (O-2), os quais interagem, respectivamente, com os íons cálcio (Ca+2) e o hidrônio (H+), que sobra do hidróxido (OH-) da base, formando os compostos aluminato de cálcio [Ca(AlO2)2] e água (H2O). Observe a equação balanceada desse processo:
Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O

