Hidrólise salina para ácido forte e base fraca

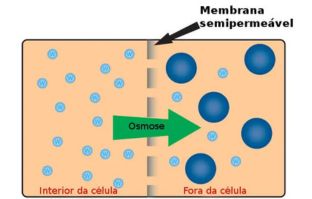
A hidrólise salina de um ácido forte e uma base fraca ocorre quando um sal (YX) é adicionado à água, e, após a sua dissociação, seu cátion (Y+) interage com o ânion hidróxido (OH-) da água. Portanto, nesse caso, não há a interação entre o ânion (X-) do sal com o cátion hidrônio (H+).
Existe apenas a interação do cátion do sal com o ânion da água porque a hidrólise só acontece entre um íon de característica fraca do sal com um íon da água. Como estamos tratando da hidrólise salina de um ácido forte e uma base fraca, isso quer dizer que o sal utilizado apresenta as seguintes características:
- Cátion capaz de formar uma base fraca, ou seja, é um elemento que não pertence às famílias IA e IIA (com exceção do magnésio) e, por isso, sofre hidrólise;
- Ânion capaz de formar um ácido forte, portanto, não sofre hidrólise.
Obs.: Formam ácidos fortes os ânions simples como o cloreto (Cl-), o brometo (Br-) e o iodeto (I-); e os ânions oxigenados sulfato (SO4-2), nitrato (NO3-), pirofosfato (P2O7-4); os halogenados como clorato (ClO3-) e perclorato (ClO4-); ânions com crômio (dicromato, Cr2O7-2, e o cromato, CrO4-2), ou manganês (maganato, MnO4-2, e permanganato, MnO4-1).
Portanto, quando vamos representar a equação química de uma hidrólise salina de um ácido forte e uma base fraca, podemos seguir um dos padrões propostos a seguir:
YX + H2O→YOH + H+ + X-
ou
Y + H2O→YOH + H+
Obs.: Como na hidrólise salina entre um ácido forte e uma base fraca, sempre existe a presença de cátions hidrônio no meio, logo o pH é sempre inferior a 7, isto é, é um meio ácido.
Exemplo da hidrólise salina entre um ácido forte e uma base fraca
O sal sulfato de alumínio [Al2(SO4)3], quando adicionado à água, sofre a seguinte dissociação:
Al2(SO4)3 + H2O→ 2Al+3+ 3SO4 -2
Assim, ele libera:
- Cátion alumínio (Al+3), que é capaz de formar base fraca (por ser da família IIA);
- Ânion sulfato (SO4 -2), que forma um ácido forte.
Portanto, nesse exemplo, ocorre uma hidrólise salina de um ácido forte e base fraca, pois o cátion (Al+3) do sal interage com ânion hidróxido (OH-) da água e forma a base Al(OH)3]. Além disso, o ânion (SO4-2) do sal não interage com o cátion hidrônio (H+) da água.
A equação química que representa a hidrólise desse sal, com componente de ácido forte e base fraca, é:
1 Al2(SO4)3 + 6 H2O→ 2 Al(OH)3 + 3 H+ + 3 SO4-2
ou
2 Al+3 + 6 H2O→ 2 Al(OH)3 + 3 H+
Fórmula para o cálculo da constante de hidrólise salina para ácido forte e base fraca
Como na hidrólise salina entre ácido forte e base fraca, a água é o meio fundamental (constante), e na solução final teremos as presenças de base fraca, do cátion hidrônio e do cátion do sal (comum à base), assim:
Y+ + H2O → YOH + H+
Podemos montar, então, a constante do equilíbrio químico de hidrólise (Kh) a partir da equação de acima:
Kh = [base fraca].[H+]|
[cátion]
Essa expressão pode ser escrita ainda da seguinte forma, se forem levadas em consideração a constante de ionização da água e a constante de dissociação da base:
Kh = [Kw]
[Kb]
Ferramentas Brasil Escola
Artigos Relacionados

Últimas notícias
Outras matérias