Manganês (Mn)
O manganês (Mn) é um metal de transição com número atômico 25. Ele apresenta brilho metálico característico, alta dureza e é quebradiço. Possui propriedades parecidas com o ferro, podendo sofrer processos corrosivos. Esse metal é abundante na natureza, podendo ser encontrado em muitos tipos de minerais, de onde pode ser extraído por processos de eletrólise ou reações exotérmicas de redução. Apenas um isótopo natural do manganês é conhecido.
Uma das características mais interessantes do manganês é a sua capacidade de assumir muitos estados de oxidação diferentes, proporcionando ampla diversidade de compostos químicos formados com outros elementos.
Apesar de ser frágil em sua forma pura, quando compõe ligas metálicas, o manganês é capaz de aumentar a maleabilidade e a resistência das ligas. A siderurgia é o setor que consome quase todo o manganês extraído da natureza.
O manganês é um nutriente essencial às plantas e aos animais, inclusive aos humanos, por participar do ciclo de atividade de várias enzimas, sob a forma de íons Mn2+. Na alimentação, esse nutriente pode ser obtido pela ingestão de oleaginosas, nozes, amendoins, avelãs, sementes, mariscos e alguns legumes folhosos.
Leia também: Propriedades dos metais — os fatores característicos desses elementos
Resumo sobre o manganês
-
Manganês (Mn) é um metal de transição de número atômico 25.
-
Possui aspecto metálico, sendo um metal duro e frágil na sua forma pura.
-
É suscetível à corrosão na presença de ar atmosférico e umidade.
-
O manganês é o quinto elemento mais abundante na crosta terrestre, encontrado em muitos minerais distintos, sendo o mais conhecido deles a pirolusita (MnO2).
-
A característica química mais importante do manganês é sua capacidade de assumir muitos estados de oxidação diferentes, resultando em compostos diversos.
-
O principal uso do manganês se dá na siderurgia, onde é empregado para melhorar a qualidade, a maleabilidade e a resistência de ligas metálicas.
-
Outros usos do manganês incluem a fabricação de pilhas, baterias, vidros, telhas e tijolos e seu emprego como reagente em indústrias químicas e de fertilizantes.
-
No que toca a saúde, sabe-se que o manganês é um nutriente essencial às plantas e animais, fazendo parte do funcionamento de enzimas.
-
Feijões, leguminosas, nozes, mariscos e vegetais são importantes fontes de manganês na alimentação.
Propriedades do manganês
-
Símbolo: Mn.
-
Número atômico: 25.
-
Massa atômica: 54,938 u.
-
Configuração eletrônica: [Ar] 3d5 4s2.
-
Estado físico: sólido (20 °C).
-
Ponto de fusão: 1246 °C.
-
Ponto de ebulição: 2061 °C.
-
Densidade: 7,3 g/cm3.
-
Eletronegatividade: 1,55 (escala de Pauling).
-
Série química: elementos de transição.
-
Localização na tabela periódica: grupo 7, período 4, bloco d.
-
Isótopo natural: 55Mn.
Características do manganês
O manganês (Mn) tem número atômico 25, é um metal de transição duro e quebradiço e possui coloração prateada e alto ponto de fusão. Esse elemento possui propriedades físico-químicas semelhantes às do elemento ferro, sendo inclusive suscetível a processos de corrosão. O manganês oxida superficialmente quando exposto ao ar atmosférico e sofre corrosão quando exposto ao ar úmido.
Na presença de ácidos inorgânicos, o manganês dissolve com facilidade, formando gás hidrogênio e o respectivo sal em que o manganês possui estado de oxidação +2. Ao ser aquecido, o manganês se torna mais reativo, podendo formar compostos com enxofre, fósforo, carbono, nitrogênio, iodo, silício, selênio, entre outros elementos.
O manganês metálico pode se tornar ferromagnético, isto é, imantar-se na presença de um campo elétrico. No entanto, essa não é uma característica inerente do metal, mas sim induzida por meio de um tratamento especial.
Esse elemento é abundante na natureza, o quinto maior em quantidade na crosta terrestre. É encontrado principalmente em minerais, como a pirolusita e a rodocrosita.
O manganês pode assumir até 11 estados de oxidação diferentes e formar uma infinidade de compostos. Destes, os mais estáveis são aqueles com estados de oxidação +2, +6 e +7, formando os sais de manganês (íon Mn2+), os manganatos (íon MnO42-) e os permanganatos (MnO4-). Compostos formados por manganês em estado de oxidação +7 são oxidantes muito fortes, sendo o sal permanganato de potássio (KMnO4) um dos agentes oxidantes mais utilizados em processos químicos.
Com massa atômica igual a 54,938, o manganês existe naturalmente sob a forma de um único isótopo. Em condições de laboratório, outros isótopos de manganês podem ser gerados. O isótopo artificial mais estável é o de massa atômica 53 (53Mn).
Para que serve o manganês?
Por ser um metal quebradiço, o manganês é frágil demais para ser utilizado como metal puro, mas se comporta muito bem quando participa da composição de ligas metálicas, atribuindo a elas aumento de resistência mecânica e melhora na maleabilidade e na resistência ao desgaste. Por essa razão, a principal aplicação do manganês se dá na composição de ligas metálicas. A siderurgia corresponde à maior parte da demanda por manganês, utilizando em torno de 90% do total extraído.
O aço comum contém cerca de 1% de manganês em sua composição. Quando produzido sem manganês, o aço se torna quebradiço ao ser laminado ou forjado. Outra função do manganês é converter o sulfeto de ferro (FeS), que tem baixo ponto de fusão, em sulfeto de manganês, o qual possui ponto de fusão maior, melhorando a qualidade da liga.
O aço Hadfield tem teor de manganês entre 11 e 14%. Esse material é forte o suficiente para aplicações mais robustas, como barras de prisão, trilhos de trem, barras metálicas para construções, cofres e escavadeiras. O alumínio que compõe as latas de bebidas contém cerca de 1,5% de manganês. Nesse caso, a função do manganês é melhorar a resistência à corrosão.
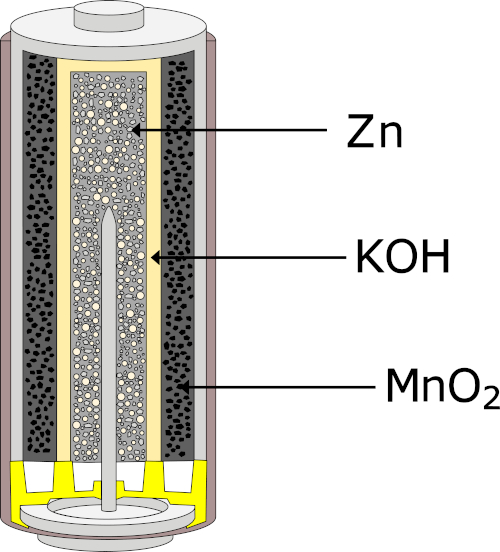
A principal aplicação não metalúrgica do manganês se dá no armazenamento de energia. Ele participa da composição de eletrodos para pilhas secas, conhecidas como pilhas zinco/carbono ou pilhas de Leclanché. O manganês também pode ser empregado em pilhas alcalinas, compostas por zinco (Zn) e dióxido de manganês (MnO2), em que hidróxido de potássio (KOH) age como eletrólito.
Na manufatura de telhas e tijolos, compostos de manganês são utilizados como pigmentos. Já o óxido de manganês tem aplicação como catalisador de reações, descolorante na fabricação do vidro e aditivo de borracha. Além disso, está presente na produção industrial de gás cloro e gás oxigênio.
O permanganato de potássio (KMnO4) tem caráter corrosivo e é fortemente oxidante, sendo empregado em grandes quantidades em processos industriais, em laboratórios químicos e em alguns tipos de tratamento de água. Até há alguns anos, o KMnO4 era utilizado como produto de limpeza caseiro e no tratamento de feridas de pele, como catapora. Esses usos não são mais indicados, pois esse composto é muito agressivo à pele. Além dos usos citados, o sulfato de manganês (MnSO4) é utilizado em fertilizantes e rações animais.
Leia também: Carbono — elemento presente nos principais ciclos biológicos existentes
Obtenção do manganês
O manganês é abundante na natureza, mas não ocorre em sua forma elementar. Ele pode ser encontrado sob a forma de óxidos e carbonatos em mais de 100 minerais diferentes, destacando-se a pirolusita, o psilomelano e a manganita. No entanto, nem todos são utilizados para a obtenção do manganês.

A tabela abaixo mostra alguns dos minerais que contêm manganês.
|
Mineral |
Composição química |
Teor de manganês |
|
Hausmanita |
Mn3O4 |
72% |
|
Pirolusita |
MnO2 |
60 – 63% |
|
Psilomelano |
(Ba, H2O)2Mn5O10 |
45 – 60 % |
|
Manganita |
Mn2O3 ‧ H2O |
62 % |
|
Rodocrosita |
MnCO3 |
47 % |
Fonte: Manganês. Recursos Minerais de Minas Gerais.
As principais minas de manganês são encontradas na Rússia, África do Sul, Austrália, Ucrânia e Geórgia. Cerca de 25 milhões de toneladas são extraídas atualmente das reservas de manganês, gerando aproximadamente cinco milhões de toneladas do metal.
No Brasil, existem duas minas de extração de manganês que concentram cerca de 90% de toda a produção do país. Elas estão localizadas em Corumbá (MS) e na Mina do Azul, no Pará. Manganês também pode ser encontrado no fundo dos oceanos, e estima-se que a quantidade do elemento sob os mares é muito superior àquela descrita para as reservas terrestres.
Como a siderurgia representa uma importante fração do setor industrial nacional, o país tem alto consumo de manganês, sendo necessário importá-lo. A nível mundial, o Brasil é o décimo colocado na lista de países importadores de manganês.
O processo de isolar o manganês dos minerais que o contêm se inicia pela solubilização da rocha em solução ácida quente, geralmente ácido sulfúrico, formando um líquido de coloração rosa que contém íons Mn2+. Em seguida, empregando o processo de eletrólise, os íons Mn2+ em solução sofrem redução à forma metálica do elemento (Mn0) e se depositam sobre o cátodo, de onde podem ser obtidos em sua forma pura. O manganês obtido por eletrólise é destinado para aplicações mais nobres, como ligas não ferrosas de alumínio, cobre, níquel e magnésio e produtos químicos de elevada pureza.
Outro método de obtenção, mais antigo, se dá por meio da calcinação dos minerais seguida da reação de redução do manganês com óxidos de sódio, magnésio ou alumínio. Esse processo gera produtos de menor pureza e é altamente exotérmico.
Alimentos ricos em manganês

A Agência Nacional de Vigilância Sanitária (Anvisa) recomenda para adultos acima de 19 anos uma ingestão de manganês de 2,3 mg por dia.
As principais fontes de manganês na alimentação são:
-
grãos integrais;
-
oleaginosas;
-
nozes;
-
sementes;
-
certos frutos do mar;
-
alguns chás;
-
vegetais folhosos e legumes específicos.
Em razão da similaridade química entre manganês e ferro, pode ocorrer no organismo uma espécie de competição de pelos sítios receptores desses íons. Por isso, alguns alimentos podem inibir a absorção de manganês no organismo — por exemplo, alimentos com alta quantidade de ácido fítico, como os feijões, e produtos de soja e de ácido oxálico, como o repolho e o espinafre.
A tabela abaixo indica os valores médios de manganês que podem ser encontrados em alimentos, considerando porções de uma xícara.
|
Alimento |
Quantidade de manganês / mg |
|
Nozes |
7,872 |
|
Mirtilo |
7,337 |
|
Avelãs |
7,101 |
|
Farinha de arroz |
6,341 |
|
Sementes de abóbora |
5,298 |
|
Moluscos |
5,1 |
|
Feijão-azuqui |
3,408 |
|
Amendoim |
2,608 |
|
Alho |
2,274 |
|
Feijão-preto |
2,056 |
|
Arroz |
2,013 |
|
Amoras |
1,847 |
|
Farinha de cevada |
1,530 |
|
Espinafre |
1,154 |
|
Chás |
0,931 |
Fonte: Departamento de Agricultura dos Estados Unidos.
Papel biológico do manganês
O manganês possui importante papel para animais, seres humanos e vegetais. Trata-se de um nutriente essencial para os seres vivos, pois faz parte de uma diversidade de processos enzimáticos.
Nos vegetais, participa do crescimento e assimilação de nitratos nas plantas verdes e nas algas. Muitas enzimas contêm átomos de manganês, como as utilizadas no processo de fotossíntese, com ação de converter moléculas de água em oxigênio.
De modo geral, os solos são deficientes em manganês. Porém, como este é um elemento importante para a saúde das plantas, é normalmente adicionado aos fertilizantes e às rações de animais em pastejo.
Nos humanos e animais, o manganês faz parte do ciclo de funcionamento de diversas enzimas, participando de processos de síntese do colesterol e dopamina, por exemplo. No organismo humano, a ingestão adequada de manganês auxilia na composição e fortalecimento dos ossos e faz parte do processo de assimilação da vitamina B1.
A forma do manganês biologicamente útil ocorre em estado de oxidação +2. Sob outras formas e em altas concentrações, o manganês pode ser tornar tóxico, afetando o cérebro e o trato respiratório. Alguns sintomas de intoxicação por manganês são esquecimento, alucinações, danos neurais, Parkinson, embolia pulmonar e bronquite.
Leia também: Selênio — outro elemento essencial à saúde humana
História do manganês
Os compostos de manganês já eram utilizados pelos humanos antes mesmo de o elemento químico em si ser descoberto. Os primeiros registros são do uso do mineral pirolusita como tinta preta em pinturas rupestres de 30.000 anos, na França.

Egípcios e romanos já utilizavam o manganês como descolorante e corante de vidros, prática que ainda é realizada atualmente.
No século XVIII, o gás cloro foi descoberto de forma acidental pela reação entre MnO2 e uma mistura de ácido sulfúrico e cloreto de sódio. Assim, o uso do manganês na produção em larga escala do gás cloro e de soluções alvejantes foi a primeira aplicação industrial do elemento.
Porém, apenas em 1774 o manganês foi reconhecido como elemento, pelo químico suíço Carl Wilhelm Scheele, e isolado, sob a sua forma metálica, pelo químico e mineralogista sueco Johan Gottlieb Gahn. Nesse experimento, Gahn colocou em um frasco de reação MnO2, óleo e carvão, fechou o frasco e o aqueceu durante algum tempo. Ao final, verificou que dentro dele havia uma massa metálica muito semelhante ao ferro, que era o manganês.
No início do século XIX, os pesquisadores começaram a desenvolver formas de melhorar as propriedades do aço e a testar diferentes proporções entre os metais constituintes da liga. As primeiras patentes que indicam o uso do manganês em aço datam de 1800.
Em torno de 1850, o aço era produzido pelo processo de Bessemer, procedimento desenvolvido por Henry Bessemer. Porém, a qualidade da liga metálica ainda não era boa o suficiente para usos estruturais em razão do excesso de carbono, naturalmente presente por causa dos minérios de ferro. Para resolver isso, em 1856 Bessemer começou a inserir excesso de oxigênio à liga metálica fundida. A ideia era que o oxigênio removesse o excesso de carbono por meio da geração do gás CO2, que pode ser facilmente retirado. Contudo, um novo problema foi gerado: oxigênio residual permanecia na liga e a tornava impura.
Ao mesmo tempo, Robert Mushet testava a fabricação do aço por meio de uma mistura entre compostos de ferro, carbono e manganês. A proposta da adição do manganês incluía remover o oxigênio e reduzir o teor de aço do ferro fundido. A ideia deu certo e resolveu o problema do processo de Bessemer.

Mushet nunca foi reconhecido de forma justa pela sua contribuição ao processo, apenas recebendo uma pensão em dinheiro de Bessemer durante os tempos finais de sua vida. As alterações na produção do aço tiveram um reflexo econômico importante na época, diminuindo o custo e o tempo dessa produção e auxiliando na expansão das ferrovias e da indústria siderúrgica.
A origem do nome manganês faz referência à região de Magnésia, território que atualmente faz parte da Grécia. Nessa região, havia dois minerais de cor preta, que os populares chamavam de magnes. Um deles era a magnetita (Fe3O4) e o outro era a pirolusita (MnO2), que apesar de possuírem a mesma aparência negra, tinham propriedades diferentes. Com o tempo, para diferenciar um do outro e também para distingui-los de outros compostos como a magnésia (MgO), o termo magnes foi sofrendo alterações até se tornar manganês.
Créditos da imagem
[1] thipjang / Shutterstock

