Mercúrio (Hg)
O mercúrio é um metal branco-prateado de elevada densidade, sendo o único elemento metálico no estado líquido, em temperatura ambiente. Outra característica marcante do mercúrio é sua alta toxicidade, principalmente quando forma compostos orgânicos, como o metilmercúrio, o qual interage com tecidos e órgãos, podendo ser bioacumulado nos organismos vivos.
Em razão da toxicidade, as aplicações do mercúrio vêm sendo desincentivadas. Atualmente, o mercúrio é usado na fabricação de lâmpadas fluorescentes, de pilhas e baterias, alguns tipos de medicamentos e de fungicidas e na fabricação do PVC.
Leia também: Níquel — um importante elemento químico cujo excesso pode causar efeitos nocivos
Resumo sobre mercúrio
-
O mercúrio é um elemento químico de número atômico 80, pertencente ao grupo 12 da Tabela Periódica.
-
É o único elemento metálico líquido em temperatura ambiente.
-
Possui coloração branco-prateada e é de alta densidade.
-
É um metal de elevada toxicidade.
-
Pode existir na forma elementar e constituindo compostos orgânicos e inorgânicos.
-
O metilmercúrio é uma forma orgânica de elevada toxicidade, pois é armazenado nos tecidos gordurosos do corpo.
-
O mercúrio é encontrado na natureza, principalmente na forma do mineral cinábrio.
-
É usado em lâmpadas fluorescentes, na extração de ouro pela formação de amálgamas, na produção do PVC, entre outros.
-
A contaminação por mercúrio é grave e pode levar à morte; promove alterações intestinais e neurológicas.
Propriedades do mercúrio
-
Símbolo: Hg
-
Número atômico: 80
-
Massa atômica: 200,592 u
-
Configuração eletrônica: [Xe] 4f14 5d10 6s2
-
Estado físico: líquido (20 °C)
-
Ponto de fusão: -38,8 °C
-
Ponto de ebulição: 356,6 °C
-
Densidade: 13,55 g/cm3
-
Eletronegatividade: 1,9 (escala de Pauling)
-
Série química: metal de transição
-
Localização na Tabela Periódica: grupo 12, período 6, bloco d.
-
Isótopos naturais: 196Hg (0,15%), 198Hg (9,97%), 199Hg (16,87%), 200Hg (23,10%), 201Hg (13,18%), 202Hg (29,86%), 204Hg (6,87%).
Características do mercúrio
O mercúrio é o único metal líquido em temperatura ambiente, possui coloração branco-prateada e escurece ao ser exposto à atmosfera. A palavra mercúrio é uma tradução do latim e significa “prata líquida”. Há indícios históricos de que esse elemento já era conhecido no Egito e no Oriente em 1500 a.C.
O mercúrio forma ligas metálicas líquidas com cobre, estanho, zinco e ouro, chamadas amálgamas.
O mercúrio é extremamente tóxico. A contaminação por esse elemento pode ocorrer pela inalação do vapor, ingestão de compostos contendo mercúrio ou por absorção cutânea.
Sete isótopos estáveis do mercúrio são conhecidos, sendo o mercúrio-202 o mais abundante, representando quase 30%.
O mercúrio pode se apresentar sob a forma metálica (ou elementar) ou na forma de compostos inorgânicos e orgânicos, assumindo estados de oxidação +1 e +2.
Os sais mais comuns de mercúrio são formados com cloretos, originando o calomelano (Hg2Cl2), e com sulfetos, formando o sulfeto de mercúrio (HgS).
Dentre os compostos orgânicos, destaca-se o metilmercúrio (CH3Hg), sendo este uma das formas mais tóxicas em razão da sua capacidade de bioacumulação.
A bioacumulação é o processo de acumulação de uma substância em tecidos ou órgãos de um organismo. Compostos orgânicos de mercúrio também sofrem biomagnificação, ou seja, se acumulam progressivamente de um nível trófico para outro da cadeia alimentar. Dessa forma, predadores têm tendência a acumular mais mercúrio do que suas presas.
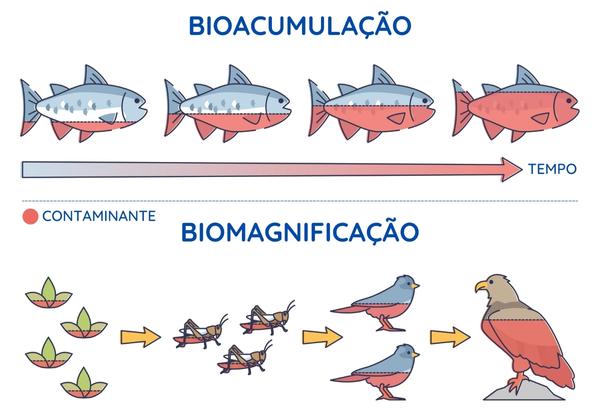
Onde se encontra o mercúrio?
O mercúrio é encontrado na crosta terrestre, em quantidade média de 0,08 gramas por tonelada de rocha.
Há cerca de 25 minerais conhecidos que contêm mercúrio, mas a extração apenas é economicamente viável por meio do cinábrio (HgS) ou sulfeto vermelho, formado por cerca de 86% de mercúrio. O cinábrio pode ocorrer sozinho ou em associação com o antimônio, ouro, ferro e zinco.
Os depósitos de mercúrio são pequenos e irregulares, geralmente ocorrendo como veias. Em razão disso, a mineração em larga escala é difícil.

Em regiões vulcânicas ou com fontes termais pode ocorrer a presença de mercúrio nativo. Ligas metálicas muito raras com mercúrio podem ser encontradas na natureza, formadas por prata, paládio e ouro.
A China concentra quase 90% do mercúrio disponível no planeta, que, na maioria das vezes, é obtido como subproduto da mineração do ouro. Outras regiões mineradoras de mercúrio são o Chile, Quirguistão, Espanha, Eslovênia, Itália, Peru e Estados Unidos.
Como se obtém o mercúrio?
As formas tradicionais de obtenção do mercúrio derivam da sua propriedade de volatilidade em baixa temperatura (comparado a outros metais).
Desse modo, uma das formas de obtenção do mercúrio ocorre por meio do aquecimento do cinábrio em um forno, com fornecimento de ar atmosférico, estando o forno em temperatura aproximada de 700 °C. Nesse caso, o mercúrio se desprende na forma de vapor, deixando dióxido de enxofre:
\(\mathbf{HgS\ (s)+ O_2\ (g)⟶Hg\ (v)+SO_2\ (g)}\)
No aquecimento do cinábrio sem oxigênio, há a sua decomposição em, aproximadamente, 740 °C, restando enxofre em estado líquido.
\(\mathbf{HgS\ (s)⟶Hg\ (v)+S\ (l) }\)
Os vapores de mercúrio são condensados pela redução de temperatura e escoados através de tubos de vidro, obtendo-se o metal puro. Em razão da elevada toxicidade, esses métodos de volatilização têm sido substituídos por métodos mais seguros.
Uma forma menos perigosa é a solubilização do cinábrio em solução de hipoclorito de sódio, sendo o mercúrio recuperado por precipitação com zinco ou alumínio ou, ainda, por eletrólise.
Aplicações do mercúrio
O mercúrio teve muitas aplicações ao longo da história, principalmente quando não se conhecia sua toxicidade, e seus derivados ainda possuem aplicações na atualidade. A dilatação térmica do mercúrio com rápida expansão e a sua baixíssima interação com o vidro o tornaram o principal elemento utilizado na construção de termômetros. No Brasil, desde 2019 é proibida a comercialização de termômetros com mercúrio, em razão de sua toxicidade. Além dos termômetros, barômetros e manômetros também utilizam mercúrio como indicador.
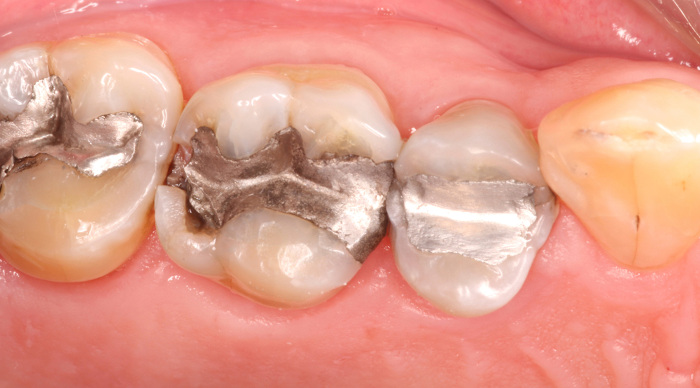
Como vimos, o mercúrio forma ligas metálicas líquidas com alguns elementos, que recebem o nome de amálgamas. A amálgama mercúrio-prata foi muito utilizada em tratamentos odontológicos e atualmente está em desuso. Além disso, a formação de amálgamas de prata e ouro com mercúrio é utilizada no processo de extração de prata e ouro de minérios.
A condutividade elétrica desse metal o faz ser empregado em interruptores, lâmpadas fluorescentes, lâmpadas emissoras de ultravioleta, lâmpadas de vapor de mercúrio, pilhas e baterias.

Alguns tipos de fungicidas agrícolas, e até mesmo alguns medicamentos contêm mercúrio na composição.
Até o século XX, alguns procedimentos eletrolíticos de fabricação de soda cáustica e cloro ainda usavam mercúrio. Essa aplicação foi praticamente abolida no século XXI. Também no passado, o cloreto de mercúrio (I) (Hg2Cl2) foi usado em pomadas antissépticas.
O cloreto de mercúrio (II) (HgCl2) é um composto incolor, inodoro e muito tóxico. Mesmo assim é usado na agricultura como fungicida e na medicina como antisséptico em condição muito diluída. Na indústria química, atua como catalisador na fabricação do cloreto de vinila (substância que dá origem ao PVC) e de outros produtos derivados de mercúrio.
O óxido de mercúrio (II) (HgO) é empregado como fonte de mercúrio elementar para a síntese de novos compostos. Também pode ser adicionado ao grafite na composição de eletrodos de baterias de mercúrio.
Ainda, o mercúrio na forma de sulfeto (HgS) é um sólido vermelho ou preto utilizado como pigmento em tintas, plásticos e borrachas.
Precauções com o mercúrio
O mercúrio é bastante tóxico, por isso atenção deve ser dada ao seu manuseio. Os vapores de mercúrio são totalmente absorvidos pelos pulmões, atravessando com facilidade as membranas celulares, atingindo o sistema nervoso central.
O mercúrio sob a forma de íons Hg2+ em sais inorgânicos alcança a corrente sanguínea em uma taxa de 10-15%.
Os compostos orgânicos de mercúrio são completamente absorvidos no sistema digestivo em razão da sua lipossolubilidade (interação com gorduras), distribuindo-se por vários órgãos e atravessando com facilidade as barreiras hematoencefálicas e da placenta. Isso gera efeitos neurológicos e teratogênicos.
→ Contaminação por mercúrio

A contaminação por mercúrio pode ser ambiental ou ocupacional:
-
Contaminação ambiental por mercúrio: ocorre, principalmente, pelo consumo de produtos contaminados por mercúrio, como peixes e frutos do mar oriundos de regiões com altos índices desse elemento.
-
Contaminação ocupacional por mercúrio: é causada pela exposição ao mercúrio em razão de atividades de trabalho, como indústrias de baterias, tintas e lâmpadas. Trabalhadores de fontes de carvão e petróleo bem como mineradores de ouro estão sujeitos à contaminação pela inalação de vapores.
Os efeitos do mercúrio no organismo dependem da forma de exposição ao metal e da concentração. De modo geral, os sintomas de contaminação por mercúrio envolvem:
-
fraqueza, anemia e desnutrição;
-
náuseas e vômito;
-
tosse, bronquite, sensação de aperto no peito e disfunção respiratória grave (quando inalado);
-
problemas renais;
-
sabor metálico e lesões no sistema digestivo (se houver ingestão);
-
alteração cardiovascular, como hipertensão e insuficiência coronária;
-
alterações no sistema nervoso, gerando mal-estar, problemas de visão, surdez, ataxia e tremores.
Veja também: Arsênio — um elemento químico que pode levar a uma intoxicação
Os sintomas podem evoluir para alterações neurológicas graves, como irritabilidade, insônia, perda de memória, confusão mental, alucinações, quadros psicóticos, alteração da coordenação motora, depressão, entre outros. O mercúrio possui ação mutagênica e teratogênica.
História do mercúrio
Métodos de tratamentos e usos para o mercúrio possivelmente são conhecidos desde 1500 a.C., mas a utilização de diferentes termos para se referir ao metal dificulta a interpretação de artefatos históricos.
A mineração do cinábrio foi descrita no século IV a.C., existindo anotações sobre a recuperação de mercúrio por processo de destilação e condensação, além da sua comercialização na forma de cinábrio entre Espanha e Roma.
Na China no século II a.C., os alquimistas tentavam usar o mercúrio no processo de conversão de metais comuns em ouro. O folclore da Antiguidade atribuiu o poder de afastar maus espíritos e de curar doenças ao mercúrio, que então passou a ter usos terapêuticos.
No século XVII, os cientistas começaram a desenvolver equipamentos e a utilizar mercúrio na construção de termômetros, barômetros e em aplicações elétricas e químicas.
No início, todos esses processos e utilizações eram muito rudimentares, ocasionando contaminação nos trabalhadores e usuários, mesmo que à época a toxicidade do mercúrio ainda não fosse conhecida. Com o avanço tecnológico, os equipamentos passaram a reduzir a perda de mercúrio por evaporação, resultando em menor índice de doenças por envenenamento.
No século XIX, o cinábrio passou a ser usado como corante vermelho intenso em fábricas, em tintas de uso em comunidades indígenas e em guerras.
Apenas a partir do século XX, as indústrias foram analisadas mediante a capacidade de poluição por mercúrio e passaram a ser reguladas. Com isso, equipamentos e métodos mais eficientes foram desenvolvidos, reduzindo as emissões de mercúrio metálico e os despejos de resíduos com mercúrio na natureza.
Alguns desastres ambientais ocorreram ao longo das décadas pela contaminação com mercúrio. No Japão foi registrada a maior tragédia relacionada ao mercúrio em 1956, em razão dos despejos irregulares de resíduos na Baía de Minamata por uma indústria de fabricação de PVC. Estima-se que, durante 20 anos, foram despejados na natureza centenas de toneladas de metilmercúrio. Conhecido como desastre de Minamata, a contaminação da água e dos peixes afetou cerca de 20 mil pessoas, que ficaram com sequelas ou faleceram em decorrência das complicações.

Regiões onde há garimpos de ouro ilegais também são afetadas pelo mercúrio utilizado de forma não segura durante a extração. No Brasil, os estados próximos à região amazônica vêm enfrentando sérios problemas de contaminação de rios, peixes, alimentos, além das populações indígenas e ribeirinhas. Estima-se que, entre 2018 e 2022, cerca de 400 crianças do povo Yanomami faleceram em decorrência da contaminação por mercúrio no território yanomami em Roraima.
Crédito de imagem
[1] JJ Harrison / Wikimedia Commons (reprodução)

