Nomenclatura dos hidrocarbonetos
A nomenclatura para moléculas de hidrocarbonetos é estabelecida, pela União de Química Pura e Aplicada (Iupac), com regras específicas, que definem bem a estrutura de cada composto. Os hidrocarbonetos recebem um prefixo de acordo com o número de carbonos, e as ramificações e insaturações também são nomeadas e localizadas.
Os hidrocarbonetos de cadeia aberta compõem as funções alcanos, alcenos, alcadienos e alcinos, que se diferenciam pelo número de insaturações. As funções cíclicas — cicloalcano, cicloalceno, cicloalcadieno — seguem a mesma lógica, sendo que, nesse caso, os hidrocarbonetos terão cadeia fechada.
Leia também: Numeração dos carbonos na cadeia principal de hidrocarbonetos
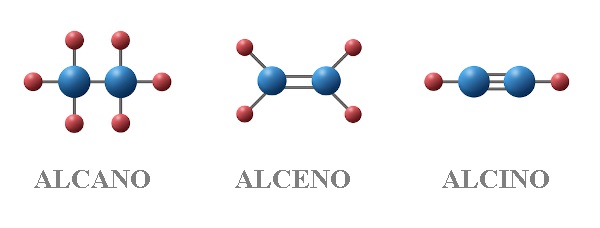
Regra geral de nomenclatura dos hidrocarbonetos
1. Definir-se a cadeia principal
Caso a molécula tenha mais de uma extremidade, isso quer dizer que se trata de uma cadeia ramificada, portanto, a cadeia principal será aquela com o maior número de carbonos lineares contendo todas as insaturações da cadeia (quando for uma molécula insaturada), o restante será ramificação.
Exemplo:
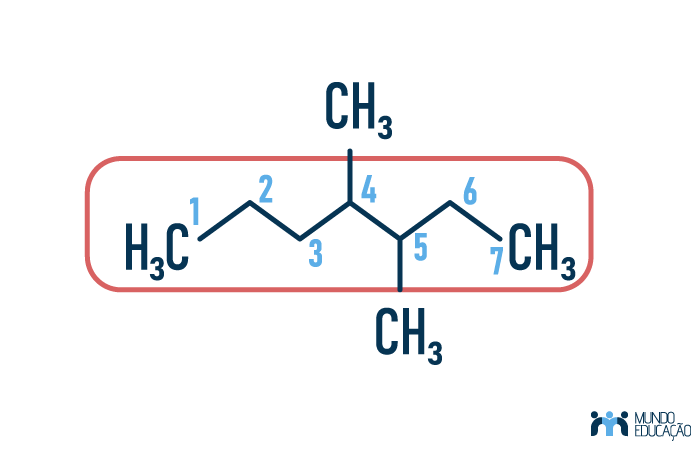
Perceba que teremos nessa molécula duas ramificações, e a cadeia principal (circulada de vermelho) terá 7 carbonos.
2. Contagem de carbonos
A contagem de carbonos da cadeia principal é usada para localizar-se as ramificações e insaturações. A regra estabelece que se deve iniciar a contagem pelo lado mais próximo da instauração e ramificação, a soma dos numerais de localização que aparecem na nomenclatura deve ser a menor possível, essa mesma contagem é usada para definir-se o prefixo da nomenclatura:
-
1 carbono: met-
-
2 carbonos: et-
-
3 carbonos: prop-
-
4 carbonos: but-
-
5 carbonos: hept-
-
6 carbonos: hex-
-
7 carbonos: hept-
-
8 carbonos: oct-
-
9 carbonos: non-
-
10 carbonos: dec-
Leia também: Classificação das cadeias carbônicas
Nomenclatura dos hidrocarbonetos ramificados
Como mencionado no tópico anterior, quando a molécula possui ramificações, o nome da ramificação precede a nomenclatura da cadeia principal, ou seja, são termos diferentes. Para nomear os radicais ou as ramificações, usaremos prefixo de acordo com o número de carbonos e terminação -il ou -ila. É necessário localizar em que carbono encontra-se a ramificação, em algumas moléculas, só haverá um local possível de existir ramificação, nesses casos, não se faz necessário localizar em que carbono encontra-se.
Exemplos:
Nomenclatura dos alcanos
A função a que pertence a molécula está diretamente ligada à terminação da nomenclatura. Alcanos são as moléculas de cadeia aberta que não possuem insaturações, e a nomenclatura para compostos dessa função será dada por:
regra geral + terminação -ano
Exemplos:
-
CH3-CH3: etano
(et- - referente ao número de carbonos na cadeia; -ano - referente à saturação da cadeia) -
CH3-CH2-CH3: propano
-
CH3-CH2-CH2-CH3: butano
Nomenclatura dos alcenos
Alcenos serão os hidrocarbonetos de cadeia aberta que possuem uma insaturação, uma dupla ligação, a nomenclatura para esse tipo de composto será dada por:
Regra geral + terminação -eno
Exemplos:
-
CH3-CH=CH2: propeno
-
CH2=CH-CH2-CH3: but-1-eno
-
CH3-CH=CH-CH2-CH3: pent-2-eno
Nomenclatura dos alcadienos
Alcadienos são os hidrocarbonetos acíclicos (cadeia aberta) que possuem duas insaturações, duas duplas ligações na cadeia. A nomenclatura para esse tipo de composto é dada por:
Regra geral + terminação -dieno
Exemplos:
-
CH2=C=CH2: propadieno
-
CH2=C=CH-CH2-CH3: pent-1,2-dieno
Nomenclatura dos alcinos
Alcinos são hidrocarbonetos insaturados com uma tripla ligação. A nomenclatura para esse tipo de molécula será dada por:
Regra geral + terminação -ino
Exemplos:
Acesse também: Classificação e nomenclatura dos haletos orgânicos
Nomenclatura dos hidrocarbonetos cíclicos
Para nomear os hidrocarbonetos cíclicos, usa-se as mesmas regras de nomenclaturas citadas, o diferencial das moléculas de cadeia fechada será o termo ciclo antes da nomenclatura referente à cadeia principal.
-
Nomenclatura dos cicloalcanos
Cicloalcanos são hidrocarbonetos de cadeia fechada insaturados, ou seja, que não possuem duplas ou triplas ligações. A nomenclatura para esse tipo de molécula será dada por:
Nomenclatura e localização da ramificação (se houver) + ciclo + regra geral + terminação -ano
Exemplo:
-
Nomenclatura dos cicloalcenos
Cicloalcenos é a função dos hidrocarbonetos de cadeia fechada que possuem uma instauração, uma dupla ligação. A nomenclatura para esse tipo de molécula será dada por:
Nomenclatura e localização da ramificação (se houver) + ciclo + regra geral + terminação -eno.
Exemplo:
-
Nomenclatura dos cicloalcadienos
Função composta por moléculas de hidrocarbonetos com duas instaurações, duas duplas ligações. A nomenclatura para esse tipo de molécula será dada por:
Nomenclatura e localização da ramificação (se houver) + ciclo + regra geral + terminação -dieno
Exemplo:
Nomenclatura dos aromáticos
Um composto aromático não segue as mesmas regras dos demais hidrocarbonetos, recebendo nome específico. Um hidrocarboneto aromático será aquele com:
-
cadeia fechada;
-
insaturação;
-
ligações conjugadas, ou seja, as insaturações alternam-se entre simples e duplas.
A aromaticidade de um composto é marcada pela transição de elétrons entre os carbonos. O benzeno é um dos hidrocarbonetos aromáticos mais citados, a nomenclatura para os compostos aromáticos derivados dele será dada de acordo com o posicionamento dos substituintes:
-
Substituintes na posição 1,2: orto
-
Substituintes na posição 1,3: meta
- Substituintes na posição 1,4: para
Exemplos:
Exemplos de hidrocarbonetos aromáticos:
Veja também: Nomenclatura de compostos com funções mistas
Exercícios resolvidos
Questão 1 – O etano é o mais simples dos hidrocarbonetos saturados, contém dois carbonos, é de grande valor comercial devido a sua aplicação industrial na produção de etileno. Qual estrutura, a seguir, corresponde a uma molécula de etano?
A)
B)
C)
D)
E)
Resolução
Alternativa D. Levando em consideração o enunciado da questão, que diz “o etano é o mais simples dos hidrocarbonetos SATURADOS, CONTÉM DOIS CARBONOS”, teremos apenas a letra D condizendo com essa descrição. Assim já eliminamos todas as demais alternativas, que possuem 3 carbonos e/ou hidrocarbonetos insaturados, ou seja, que possuem dupla ligação.
Questão 2 – Hidrocarbonetos são compostos orgânicos constituídos apenas de carbonos e hidrogênios, podem ser saturados ou não, de cadeia aberta ou fechada. Essas características definem a função a que pertence determinada molécula. Sobre o composto a seguir, assinale a alternativa que contém a nomenclatura e função correspondente.
-
2-metil-pent-2,4-ino
-
3-metil-hex-1,3-dieno
-
3-metil-pent-1,2-ino
-
3-etil-pent-1,3-dieno
-
3-metil-pent-1,3-dieno
Resolução
Alternativa E. Analisando a molécula, podemos ver que:
-
A cadeia principal, aquela que contém todas as ramificações e o maior número de carbonos lineares, tem 5 carbonos, ou seja, prefixo -pent.
-
Existe uma ramificação com 1 carbono, localizada no carbono 3 da cadeia principal, portanto: 3-metil.
-
Como são duas instaurações, duas duplas ligações, sabemos que se trata de um composto da função ALCADIENO, e o sufixo do composto localizando as instaurações será: 1,3-dieno.
Juntando as informações, e de acordo com as regras da Iupac, temos: 3-metil-pent-1,3-dieno.



