Hidrólise
Hidrólise é o nome dado ao processo químico no qual moléculas de substâncias são quebradas em unidades menores a partir da ação de íons (cátions e ânions) provenientes da ionização da água.
Hidrólise salina
Hidrólise salina é um fenômeno químico em que os íons provenientes da dissociação de um sal dissolvido na água interagem com os íons da água, formando um ácido e/ou uma base fraca.
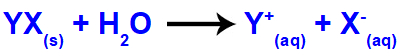
Equação que demonstra os íons provenientes de um sal qualquer.
A hidrólise salina ocorre quando o cátion hidrônio (H+) interage com o ânion do sal (X-), formando um ácido fraco. Esse processo também ocorre quando o cátion (Y+) do sal interage com o ânion hidróxido (OH-), formando uma base fraca.
Base fraca
Uma base é fraca quando formada por elementos que não pertencem às famílias dos metais alcalinos e metais alcalinoterroros.
Ácidos fracos
São considerados fracos os ácidos que não são hidrácidos (ácidos sem O, HCl, HBr, HI e HF). Oxiácidos cuja subtração da quantidade de oxigênios pela quantidade de hidrogênios resulte em zero também são ácidos fracos.
Veja também: Força ácida
Hidrólise de proteínas
A hidrólise de uma proteína ocorre quando suas unidades de aminoácidos são separadas umas das outras pela quebra da ligação peptídica existente entre elas. Isso ocorre em decorrência da ação da água e de algum outro agente.
.jpg)
Representação da ligação peptídica entre dois aminoácidos.
Por ser muito forte, a ligação peptídica não pode ser quebrada somente pela água. Assim, é necessário o auxílio de um agente com teor ácido capaz de auxiliar a quebra. No organismo humano, as enzimas desempenham esse papel. Em laboratório, além das enzimas, podem ser usados ácidos fortes, como o ácido clorídrico.
Exemplo:
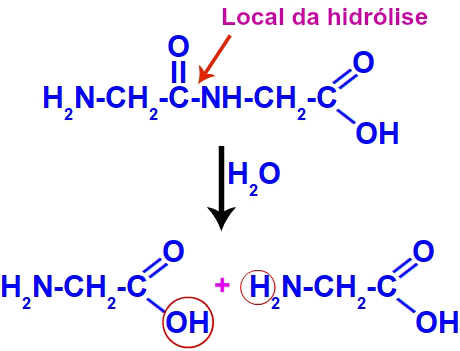
Representação da hidrólise de uma ligação peptídica.
Na hidrólise da proteína acima, o ácido e o aquecimento, juntamente com os íons da água, promovem a quebra da ligação peptídica. Em seguida, o hidróxido liga-se ao carbono, formando uma carboxila, e o hidrogênio liga-se ao nitrogênio.
Como resultado da hidrólise da proteína acima, ocorre a liberação de duas moléculas do aminoácido glicina. Vale ressaltar que os aminoácidos apresentam grande importância para o organismo humano, como controle do sistema imunológico e produção do hormônio do crescimento.
Veja também: A química das proteínas
Hidrólise e desidratação
Tanto a hidrólise quanto a desidratação são fenômenos químicos que envolvem a presença de moléculas de água. Existe, porém, uma grande diferença entre essas reações: na hidrólise, ocorre a quebra de moléculas pela ação da água, já na desidratação, ocorre a formação de moléculas de água.
Como vimos anteriormente, a hidrólise pode ser enzimática ou ácida, já a desidratação pode ser intermolecular ou intramolecular.
-
Desidratação intramolecular: ocorre quando a molécula de água é formada a partir da retirada de uma hidroxila e de um hidrogênio de uma única molécula:
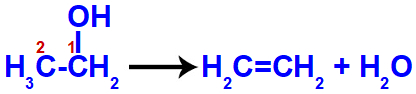
-
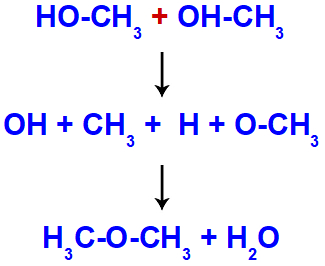
Desidratação intermolecular: ocorre quando a molécula de água é formada a partir da retirada de uma hidroxila de uma molécula e do hidrogênio de outra molécula:
Hidrólise na Biologia
A hidrólise está relacionada com o metabolismo dos seres vivos, principalmente com as reações químicas que envolvem a presença de enzimas. Veja abaixo algumas enzimas que participam de processos digestivos:
-
Digestão de carboidratos: sacarase (quebra a sacarose em glicose e frutose), maltase (quebra a maltose em duas moléculas de glicose);
-
Digestão de proteínas: protease (quebra a molécula da proteína em aminoácidos);
-
Digestão de lipídios: lipase (quebra as moléculas dos lipídios em moléculas de colesterol, ácidos graxos e glicerol).
Veja também: Saliva
A hidrólise enzimática dos nutrientes leva à formação de moléculas menores, as quais são utilizadas pelo organismo para diversas ações biológicas, como produção de energia e de anticorpos.
Outro exemplo de hidrólise na Biologia é a hidrólise do ATP (Adenosina Trifosfato), que é fundamental para a produção de energia livre para o organismo, favorecendo o funcionamento de todos os sistemas fisiológicos.
Resumo
-
Hidrólise é a quebra de uma molécula maior em moléculas menores na presença de água.
-
Hidrólise salina ocorre quando um sal apresenta cátion de base fraco ou ânion de ácido fraco.
-
A hidrólise das proteínas degrada essas macromoléculas em unidades menores, os aminoácidos.
-
A hidrólise das proteínas pode ocorrer na presença de um ácido ou de uma enzima.
-
Desidratação é uma reação em que uma molécula de água é retirada de uma única molécula (intramolecular) ou de um par delas (intermolecular).
-
A hidrólise está presente no metabolismo e na digestão dos nutrientes.
Exercício sobre hidrólise
Exercício 1- (U. Ribeirão Preto) Quanto às proteínas, podemos afirmar corretamente que:
a) Duas proteínas que originam os mesmos aminoácidos por hidrólise, nas mesmas proporções, podem não ser iguais.
b) Desnaturação significa ligação entre aminoácidos e é uma síntese por desidratação.
c) A estrutura terciária de uma proteína determina sua forma, mas não interfere na sua função ou especificidade.
d) Além da importante função estrutural, as proteínas também são as mais importantes substâncias de reserva energética e de defesa.
e) O colágeno e a elastina são componentes contráteis das células musculares e deslizam, gerando movimentos.
Resposta: letra a)
Proteínas que dão origem aos mesmos aminoácidos não são, necessariamente, iguais.
b- Desnaturação é a perda da estrutura (secundária, terciária ou quaternária) de uma proteína.
c- Toda estrutura de uma proteína interfere na sua função.
d- As proteínas não são substâncias de reserva energética.
e- Os componentes contráteis das células musculares são elastina, fibrila e miofibrila.