Reações de eliminação
Reações de eliminação são o processo em que ocorre a quebra de uma molécula, desvinculando uma das partes do composto. Para que a reação aconteça, é necessária a presença de um catalisador específico para cada tipo de reação e molécula.
Temos quatro tipos de reações de eliminação:
- desidrogenação;
- de-halogenação;
- de-halogenidretos;
- desidratação.
As reações de eliminação são muito importantes para diferentes tipos de segmentos industriais, considerando-se que matérias-primas, como o polietileno e o isopor, são advindas delas.
Leia também: Classificação das cadeias carbônicas – como fazer?
Como ocorrem as reações de eliminação?
A reação de eliminação ocorre de forma inversa à reação de adição a alcenos. Naquela temos como produto uma molécula menor que o reagente, pois, quando submetemos o composto original aos efeitos de um catalisador e outros agentes necessários a esse processo, ele perde partes de sua molécula. Existem quatro tipos de reação de eliminação, veja como funciona cada um deles nos tópicos a seguir.
Tipos de reações de eliminação
-
Reação de desidrogenação
Para que haja a desidrogenação de uma molécula, usamos calor como catalisador. Nesse tipo de reação, temos como molécula inicial um alcano, que, após o processo, torna-se um alceno.
Veja o exemplo a seguir:
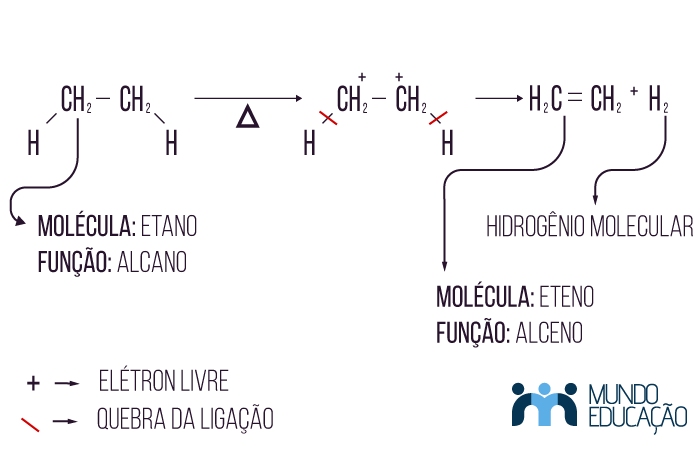
Repare que cada um dos carbonos perde uma ligação de hidrogênio, ficando, assim, com um elétron livre cada, o que possibilita a formação de uma dupla ligação entre eles. Assim teremos ao final da reação uma molécula insaturada (alceno), e hidrogênio no estado gasoso.
Leia também: Reações de substituição no benzeno
-
Reação de de-halogenação
Nessa reação ocorre a retirada de dois halogênios de um hidrocarboneto, sendo que eles precisam estar situados em carbonos vizinhos (dialeto vicinal). Para que ela ocorra, será necessário zinco e álcool como catalisadores. Assim como na reação de hidrogenação, teremos aqui uma instauração após a retirada dos átomos, consequentemente, teremos como resultado uma molécula de alceno.
Exemplo:
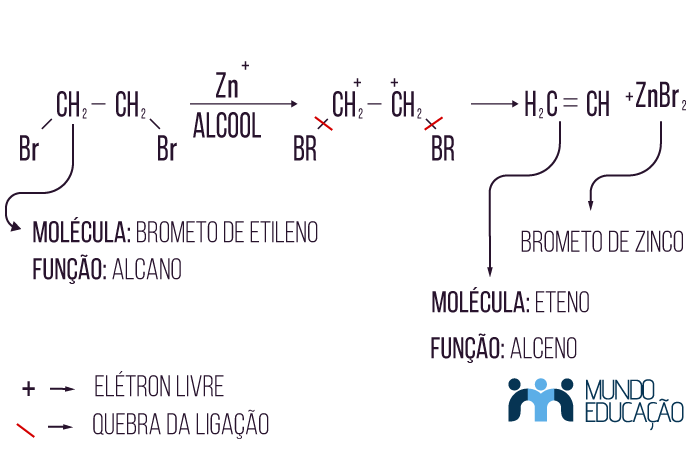
Observe que o bromo é um átomo eletronegativo e que o zinco é eletropositivo, ocorre, portanto, a atração entre eles, formando-se uma molécula de ZnBr2 (brometo de zinco).
-
Reação de desidro-halogenação
Desidro-halogenação, como a palavra sugere, é a retirada ou eliminação de um hidrogênio e um halogênio ligados a um hidrocarboneto. Essa eliminação é feita usando-se de uma base de caráter forte e álcool, por exemplo, uma potassa alcoólica. Acontece, nesse caso, a atração entre a base KOH e o ácido proveniente da união entre o halogênio e o hidrogênio retirados da molécula inicial. Veja o passo a passo a seguir:
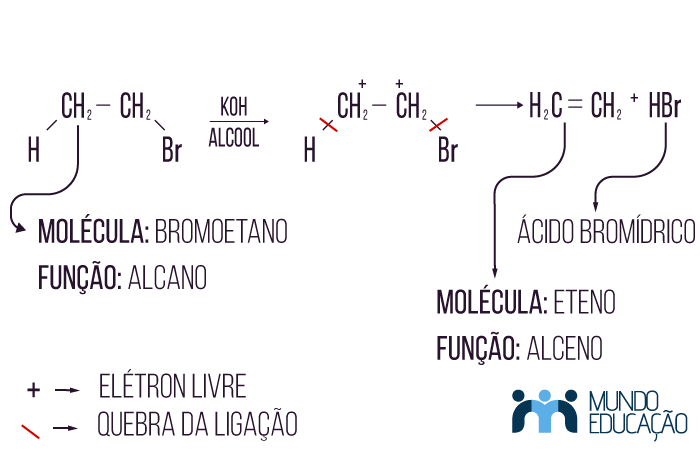
Atenção: Se nossa molécula inicial tiver mais de dois carbonos, teremos a formação de dois produtos diferentes, isômeros. Entretanto um produto estará em maior quantidade, e, para sabermos qual será ele, usaremos a regra de Zaitsev: o hidrogênio a sair na reação de eliminação será o do carbono menos hidrogenado. Lembrando que, por questão de equilíbrio eletrônico da molécula, os carbonos em questão são os dois vizinhos do carbono que tem como ligante o halogênio. Observe o exemplo:
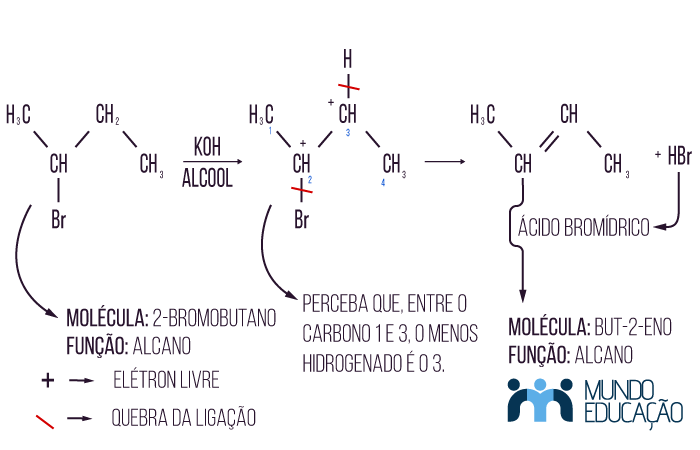
Acesse também: Halogenação de alcanos – reação orgânica de substituição
-
Reação de desidratação
Para essa reação de eliminação, teremos a retirada de H2O, submetendo o sistema a uma temperatura de 140 °C ou 170 °C (varia de acordo com o tipo de reação) e em presença de ácido sulfúrico. Estudaremos aqui a reação de desidratação em álcool e ácidos carboxílicos, sendo que essa reação pode ocorrer de forma intramolecular (uma molécula) ou intermolecular (entre duas moléculas). Veja, a seguir, um exemplo para cada um dos casos:
-
Desidratação em álcool
→ Intramolecular
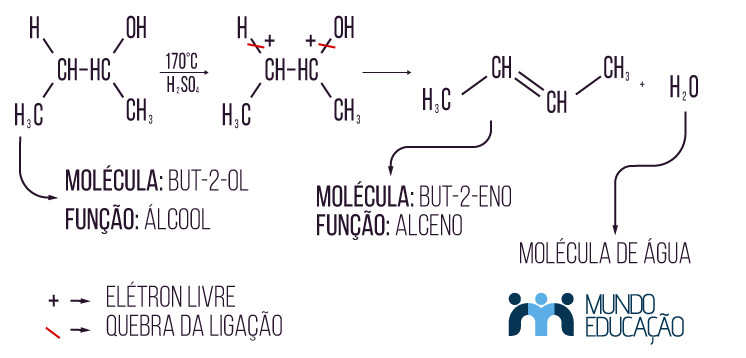
Observe que nessa reação foi aplicada a regra de Zaitsev, portanto, demonstramos seu produto predominante.
→ Intermolecular
Nesse caso participam como reagentes duas moléculas da função álcool, de uma delas se desprende uma hidroxila (OH), e da outra, um hidrogênio (H). Esse tipo de desidratação resulta em uma molécula de éter. Para essa reação de eliminação, usa-se temperatura de 140 °C e ácido sulfúrico. Veja o exemplo a seguir:
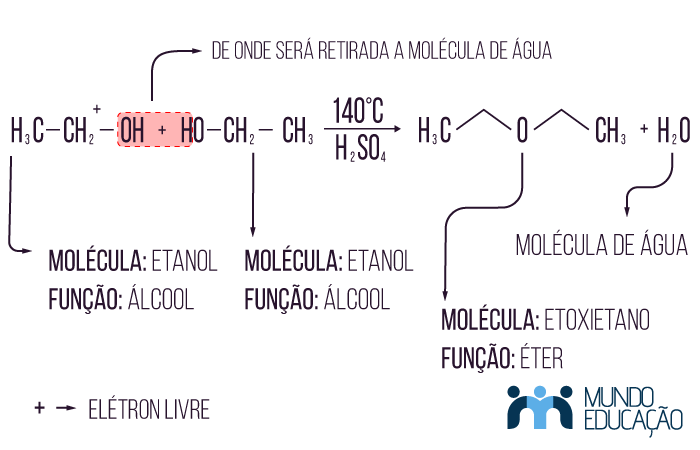
Leia também: Reações de hidratação em alcinos – conheça o processo
-
Desidratação em ácidos carboxílicos
Como produto da reação de desidratação de ácidos carboxílicos, teremos os anidridos. Para esse tipo de desidratação, será feito aquecimento do sistema e uso e óxido de fósforo, que é um poderoso dessecante. Vamos às reações:
→ Intramolecular
A reação de desidratação intermolecular acontece com um diácido, um ácido carboxílico com duas carboxilas, formando um anidrido cíclico. Observe o exemplo:
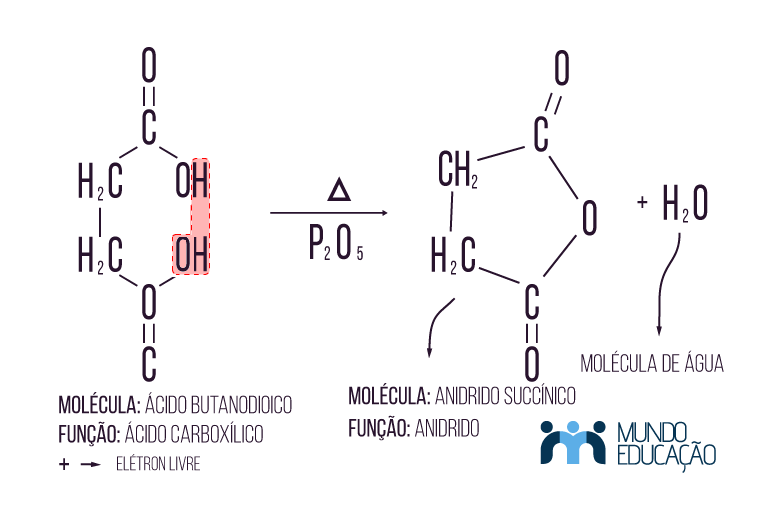
→ Intermolecular
Nesse caso a reação de desidratação acontece entre duas moléculas de ácido carboxílico, em que teremos como produto da reação uma molécula de anidrido alifático e uma molécula de água.
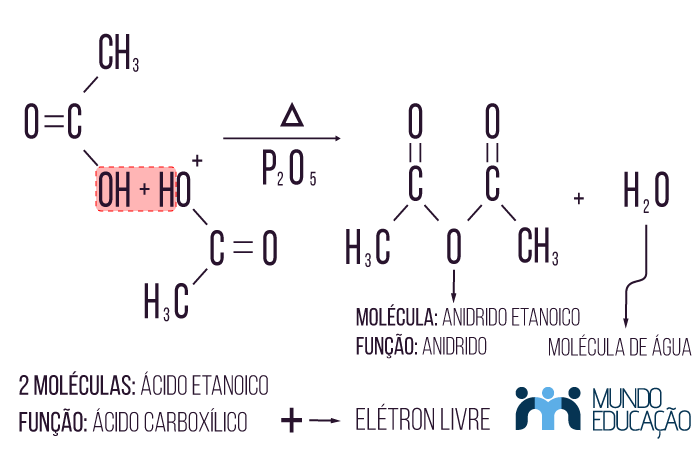
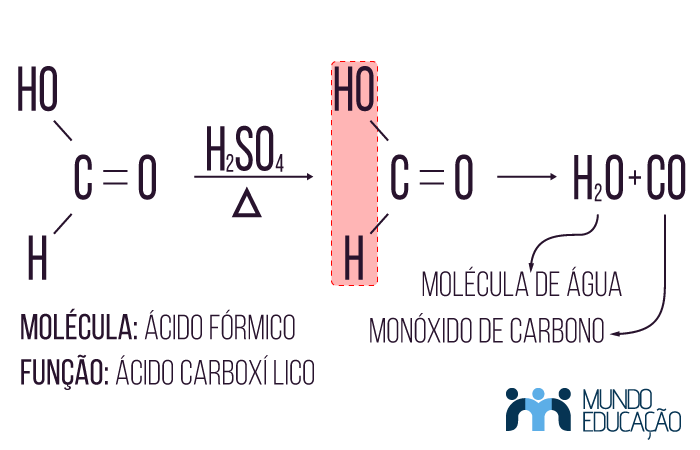
Existe uma exceção à regra de formação dos anidridos, que é o ácido fórmico, esse composto passa pela desidratação nas mesmas condições citadas e tem como produto da reação o monóxido de carbono e água.
-
Reação de eliminação e substituição
Nas reações de substituição, teremos quebras de ligações e retirada de hidrogênio, halogênio e outros elementos ou grupos moleculares, assim como nas reações de eliminação. No entanto, o propósito é outro, o produto procurado em uma reação de substituição é totalmente diferente do encontrado em reações de eliminação, pois, para que ocorra a substituição na cadeia carbônica após a quebra da ligação, outro elemento ou complexo dará lugar ao elemento que saiu da molécula original.
Resumo sobre reações de eliminação
- Reação de eliminação: quando acontece a quebra de uma molécula, retirando-se partes dela. Para isso, faz-se uso de agentes e catalisadores que favoreçam a extração do composto desejado.
- Importância: essas reações são muito importantes comercialmente, pois matérias-primas, como polietileno e anidridos, são advindas delas.
- Tipos de reação de eliminação: desidrogenação, de-halogenação, de-halogenidretos ou desidratação.
- Reações de eliminação e de substituição: possuem algumas semelhanças no processo, como a quebra de ligações, no entanto, diferem-se em seus produtos resultantes e condições necessárias.

Exercícios resolvidos
Questão 1 - (Unicruz-RS). Os álcoois, por desidratação intramolecular e intermolecular, respectivamente, dão origem a:
a) éster e éter.
b) éter e aldeído.
c) alcano e éster.
d) alcano e ácido carboxílico.
e) alceno e éter.
Resolução
Alternativa E. No caso de desidratação intramolecular, uma molécula de álcool que perde uma hidroxila torna-se um alcano; perdendo também um hidrogênio, ela ganha uma instauração, forma, portanto, um alceno.
No segundo caso, em desidratação intermolecular, ou seja, entre duas moléculas de álcool, teremos que uma delas se desprende da hidroxila, e a outra, do hidrogênio. No local em que ocorreu a quebra das ligações, teremos elétrons ligantes, promovendo, portanto, a união dos dois agregados moleculares restantes após a desidratação, o que nos leva a um produto final pertencente à função éter.
Questão 2 - Em reações de de-halogenação, teremos, respectivamente, qual função no início como reagente e no fim como produto da reação?
a) álcool e éter
b) cetona e alceno
c) alcano e alceno
d) alcino e alceno
e) álcool e alceno
Resolução
Alternativa C. A reação de de-halogenação trata-se da eliminação de dois halogênios da molécula. Tratando-se de um composto orgânico, a molécula inicial, independentemente do tipo de halogênio a ser extraído, será da função alcano. Após a eliminação dos halogênios, por uma questão de equilíbrio eletrônico, acontecerá uma dupla ligação entre os carbonos que perderam seus halogênios, transformando a molécula em um alceno.
