Sais de ácidos carboxílicos
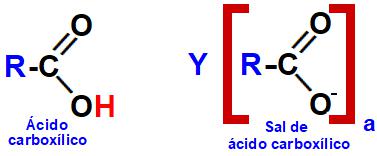
Sais de ácidos carboxílicos são compostos orgânicos oxigenados que apresentam como principal característica a presença de uma carboxila. Nessa carboxila, há substituição do hidrogênio da hidroxila (OH) por um cátion de um metal qualquer ou pelo cátion amônio (NH4+).
Representações estruturais de um ácido carboxílico e de um sal de ácido carboxílico.
1. Produção dos sais de ácidos carboxílicos
Um sal de ácido carboxílico é produzido quando um ácido carboxílico é colocado no mesmo meio reacional que uma base inorgânica (substância composta por um metal ou pelo cátion amônio associados ao grupo hidroxila) ou orgânica (como as aminas). Essa reação é denominada reação de salificação ou reação de neutralização.
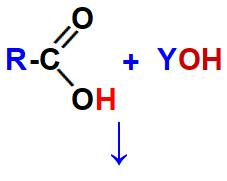
Reagentes necessários para a formação de um sal de ácido carboxílico.
Inicialmente, temos a dissociação da base, ou seja, ocorre a separação do cátion (seja ele formado por um metal ou pelo amônio) e do ânion hidróxido (OH-).
![]()
Equação que representa a dissociação da base.
Juntamente com a dissociação da base, ocorre a ionização do ácido carboxílico, ou seja, a formação do cátion hidrônio (formado a partir do hidrogênio da carboxila do ácido) e do ânion.
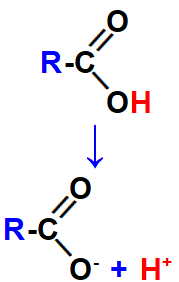
Equação que representa a ionização do ácido carboxílico.
Por fim, o cátion hidrônio interage com o ânion hidróxido, formando água, enquanto que o cátion proveniente da base interage com o ânion proveniente do ácido, formando o sal de ácido carboxílico.
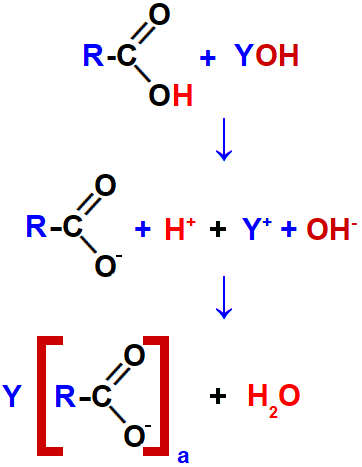
Representação da interação dos íons que formam o sal de ácido carboxílico.
Obs.: Na imagem, a é a carga do cátion Y, que interagiu com o ânion proveniente do ácido, ou seja, é a quantidade de hidroxilas da base.
Veja também: Reações de esterificação
2. Propriedades dos sais de ácidos carboxílicos
-
São compostos iônicos, ou seja, são formados por ligações iônicas;
-
À temperatura ambiente, são sólidos;
-
São inodoros;
-
Por serem iônicos, apresentam pontos de fusão e de ebulição elevados. Seus pontos de fusão são tão elevados que é mais fácil transformá-los em outras substâncias químicas, por meio de uma decomposição térmica, do que fazer o sólido virar líquido;
-
Apresentam uma extremidade polar e outra apolar, ou seja, quanto à polaridade, são compostos mistos;
-
Quando apresentam cátions de elementos da família dos metais alcalinos ou com o amônio (NH4+), são bastante solúveis em água.
3. Nomenclatura dos sais de ácidos carboxílicos
A nomenclatura de um sal de ácido carboxílico, assim como de todo composto orgânico, segue uma regra determinada pela IUPAC (União Internacional da Química Pura e Aplicada). Veja abaixo como é formado o nome de um sal de ácido carboxílico:
-
Prefixo correspondente ao número de carbonos
-
Infixo relacionado ao tipo de ligações (an, en, in, etc) entre os carbonos
-
Sufixo -oato (por ser um sal)
-
Preposição de
-
Nome do metal ou do cátion amônio.
3.1- Exemplos de nomenclatura de sais de ácidos carboxílicos
Exemplo 1: sal com dois carbonos
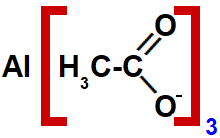
Estrutura de um sal de ácido carboxílico com dois carbonos.
Nesse exemplo, temos:
-
Dois átomos de carbono: prefixo et-
-
Apenas ligações simples entre os átomos de carbono: infixo -an-
-
Sufixo -oato
-
Preposição de
-
Metal ligado a ele: alumínio
Sendo assim, o nome desse composto é etanoato de alumínio.
Exemplo 2: sal com quatro carbonos
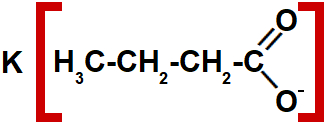
Estrutura de um sal de ácido carboxílico com quatro carbonos.
Nesse exemplo, temos:
-
Quatro átomos de carbono: prefixo but-
-
Apenas ligações simples entre os átomos de carbono: infixo -an-
-
Sufixo -oato
-
Preposição de
-
Metal ligado a ele: potássio
Sendo assim, o nome desse composto é butanoato de potássio.
Veja também: Nomenclatura dos ésteres
4. Aplicações dos sais de ácidos carboxílicos
Entre as utilizações dos sais de ácidos carboxílicos, podemos citar:
-
Constituem o princípio ativo de diversos medicamentos;
-
Fazem parte da composição de corantes para tecidos;
-
São componentes principais na produção de sabões e sabonetes.
Obs.: Os sais de ácidos carboxílicos são utilizados na produção de sabonetes e sabões porque eles apresentam, em sua cadeia carbônica, uma parte polar (capaz de unir-se à água) e uma parte apolar (capaz de unir-se à molécula de sujeira, por exemplo ao óleo na roupa).
5. Exercícios sobre sais de ácidos carboxílicos
Questão 1 - Dadas as substâncias abaixo, qual delas pode atuar como um sabão?
a) Propanona
b) Ácido butanoico
c) Etanol
d) Etanoato de metila
e) Propanoato de magnésio
Resposta: Letra e)
Uma substância pode atuar como sabão quando é um sal de ácido carboxílico. Entre as opções fornecidas, temos um sal na alternativa e, porque seu nome é formado por oato + de + nome de um metal (no caso, o magnésio).
Questão 2 - Para a formação de um sal de ácido carboxílico, é necessário qual dos pares de elétrons abaixo?
a) Ácido carboxílico e éster
b) Ácido carboxílico e álcool
c) Ácido carboxílico e amina
d) Ácido carboxílico e base inorgânica
e) Ácido carboxílico e nitrocomposto
Resposta: Letra d)
Uma reação de salificação (formação de um sal de ácido carboxílico) ocorre sempre que reagimos um ácido carboxílico com uma base inorgânica, ou seja, alternativa d.