Reações químicas
As reações químicas caracterizam a transformação da matéria, ou seja, quando algo tem sua composição química alterada para dar origem a uma substância, dizemos que ocorre uma reação química. Desse modo, elas fazem parte do nosso dia a dia, sejam externas, ocorrendo em nossa volta, como a combustão, corrosão e a fermentação; sejam internas, em cada indivíduo, nos processos bioquímicos, como a digestão de alimentos nos animais e a fotossíntese nas plantas.
Leia também: Quais são as propriedades da matéria?
Resumo sobre reações químicas
-
Reações químicas são processos em que substâncias se transformam em outras.
-
Ocorrem em condições específicas de temperatura e pressão, podendo absorver ou liberar energia durante o processo.
-
São representadas por equações químicas que mostram os reagentes e produtos.
-
O balanceamento das equações é necessário para que a quantidade de átomos seja a mesma nos dois lados da equação.
-
Podem ser de quatro tipos: síntese, decomposição, simples troca ou dupla troca.
-
São regidas por duas leis fundamentais: conservação das massas e proporções constantes.
-
São importantes na produção de materiais, na geração de energia, na indústria alimentícia, nos processos biológicos, no meio ambiente e na medicina.
Videoaula sobre reações químicas
O que são reações químicas?
Reações químicas são processos em que ocorrem mudanças na composição química de substâncias, resultando na formação de novas substâncias. Nesse sentido, essas mudanças são acompanhadas por alterações nas propriedades físicas e químicas das espécies químicas envolvidas. Em vista disso, podem envolver a quebra de ligações entre átomos e moléculas (reações de decomposição) ou a formação de novas ligações entre átomos a fim de criar moléculas (reações de síntese).
Nesse contexto, podemos citar vários exemplos de reações químicas, como:
-
Combustão: a queima de combustíveis como gasolina ou carvão é uma reação química em que o combustível reage com o oxigênio do ar para produzir dióxido de carbono e água, liberando energia.
-
Fermentação: na fermentação, micro-organismos como leveduras convertem açúcares em álcool e dióxido de carbono. Esse processo é usado na produção de bebidas alcoólicas e na fabricação de pães.
-
Oxidação de metais: a oxidação do ferro na presença de oxigênio e umidade forma ferrugem (óxido de ferro), uma reação que deteriora o metal ao longo do tempo.
-
Neutralização: a reação entre um ácido, como ácido clorídrico (HCl), e uma base, como hidróxido de sódio (NaOH), forma água e um sal, como cloreto de sódio (NaCl).
Quando ocorrem as reações químicas?
As reações químicas ocorrem quando espécies químicas (átomos, moléculas e íons) interagem umas com as outras e mudam para formar novas substâncias. Ademais, para que isso aconteça, é necessário que haja colisões eficazes entre as moléculas dos reagentes, com energia suficiente para romper as ligações químicas existentes e formar novas ligações. Chamamos isso de energia de ativação, a energia mínima necessária para iniciar a reação.
Diante disso, vejamos abaixo os principais fatores que influenciam na ocorrência de uma reação:
-
Orientação correta: além da energia, as moléculas precisam estar orientadas corretamente durante a colisão para que a quebra e a formação de ligações ocorram de maneira adequada. Se elas colidirem em uma orientação incorreta, a reação não acontece.
-
Energia de ativação: é a energia mínima necessária para iniciar a reação, logo, ela é necessária para quebrar as ligações químicas nos reagentes e iniciar a formação de novas ligações nos produtos. Além disso, o fornecimento dessa energia pode vir na forma de calor, luz ou outros tipos de energia.
-
Presença de catalisador: um catalisador é uma substância que aumenta a velocidade de uma reação química sem ser consumida na reação. Sendo assim, ele faz isso fornecendo um novo caminho de reação que requer uma energia de ativação menor. Com a presença dele, mais moléculas têm energia suficiente para reagir, aumentando a taxa de colisões efetivas e, portanto, a velocidade da reação.
Veja também: O que pode afetar a velocidade de uma reação química?
Quais são as leis das reações químicas?
As leis das reações químicas são os princípios fundamentais que governam o comportamento das substâncias durante uma reação. Nesse sentido, as duas leis principais são: a lei de conservação das massas e a lei das proporções constantes.
→ Lei da conservação das massas de Lavoisier
A massa total dos reagentes em uma reação química é igual à massa total dos produtos. Em outras palavras, a quantidade de matéria (átomos) antes e depois da reação é a mesma, apenas rearranjada. Por exemplo, a combustão do gás metano na presença de oxigênio tem como produtos dióxido de carbono e água, cuja soma das massas é igual à massa total anterior à reação, conforme ilustrado abaixo:
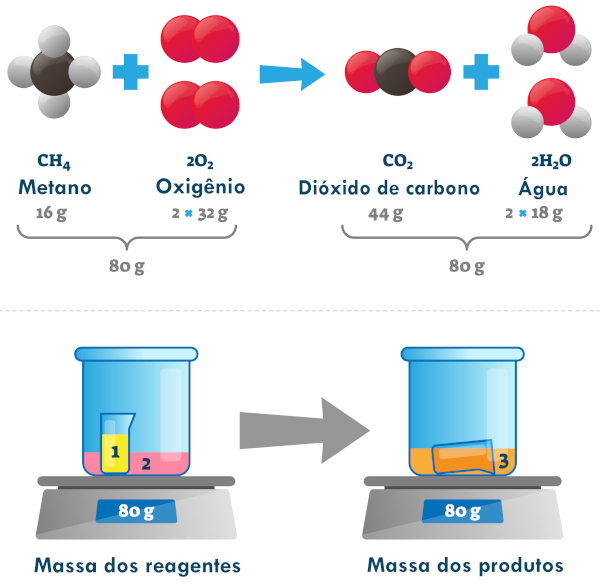
→ Lei das proporções definidas (ou constantes) de Proust
Essa lei afirma que os elementos que compõem um composto químico estão sempre presentes em proporções fixas e definidas por massa. Por exemplo, a água (H2O) sempre contém dois átomos de hidrogênio para cada átomo de oxigênio, em termos de massa, conforme ilustrado a seguir:
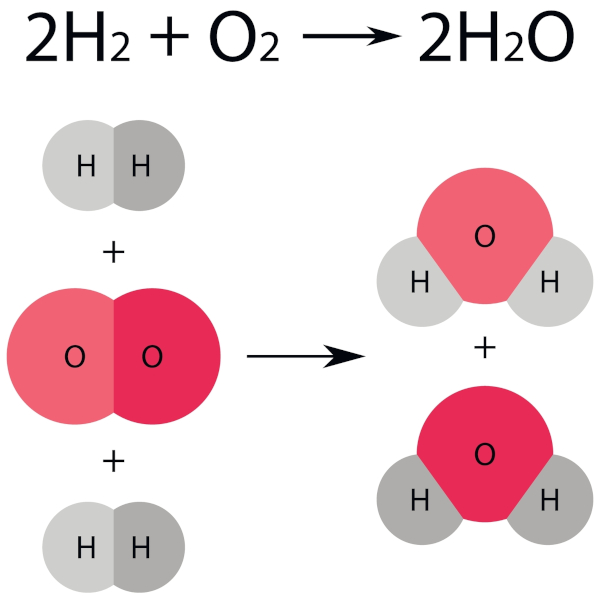
Tipos de reações químicas
Existem vários tipos de reações químicas, cada uma com características específicas. De modo geral, podemos dividi-las em quatro tipos de acordo com o rearranjo dos átomos, como: síntese, decomposição, simples troca e dupla troca.
Sendo assim, vejamos como ocorre cada uma delas:
-
Síntese: duas ou mais substâncias se combinam para formar um único produto.
Exemplo:
2 H2 + O2 → 2 H2O
O hidrogênio e oxigênio reagem para formar água.
-
Decomposição: uma substância se decompõe em duas ou mais substâncias mais simples.
Exemplo:
2 H2O → 2 H2 + O2
A água se decompõe em hidrogênio e oxigênio.
-
Simples troca: um elemento substitui outro em um composto.
Exemplo:
Zn + 2 HCl → ZnCl2 + H2
O zinco substitui o hidrogênio no ácido clorídrico.
-
Dupla troca: os cátions e ânions de dois compostos diferentes trocam de lugar.
Exemplo:
NaCl + AgNO3 → NaNO3 + AgCl
O Na+ troca de lugar com o Ag+.
Diante disso, veja abaixo um resumo com exemplos genéricos de cada tipo de reação:
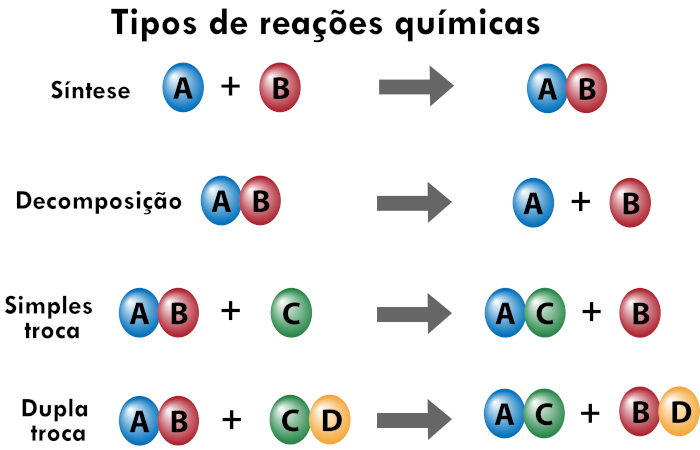
Como representar as reações químicas?
As reações químicas podem ser representadas de várias maneiras, mas uma das formas mais comuns é por meio de equações químicas, as quais se caracterizam por uma expressão que utiliza símbolos e fórmulas para representar uma reação. Diante disso, veja, a seguir, como é feita essa representação.
-
Símbolos e fórmulas
Primeiro, entenda que, em uma equação química, os reagentes são escritos à esquerda da seta (→) e os produtos à direita. Sendo assim, os símbolos representam os elementos (como H para hidrogênio e O para oxigênio), e as fórmulas representam as substâncias (como H2O para água e NaCl para cloreto de sódio).
-
Balanceamento
Nesse contexto, é importante que uma equação esteja balanceada, o que significa que o número de átomos de cada elemento nos reagentes deve ser igual ao número nos produtos. Por exemplo, a equação não balanceada:
H2 + O2 → H2O
Deve ser balanceada para:
2 H2 + O2 → 2 H2O
Portanto, a equação química balanceada indica que dois mols de moléculas de hidrogênio reagem com um mol de moléculas de oxigênio para formar dois mols de moléculas de água.
-
Fases físicas
Às vezes, as fases das substâncias são indicadas por letras entre parênteses, como (s) para sólido, (l) para líquido, (g) para gás e (aq.) para aquoso (em solução aquosa).
Exemplo: A combustão do metano (CH4) em oxigênio (O2) para formar dióxido de carbono (CO2) e água (H2O):
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(l)
-
Condições de reação
Em algumas equações, as condições de reação, como temperatura, pressão ou catalisadores, podem ser indicadas acima ou abaixo da seta. Por exemplo, a reação abaixo ocorre na presença de um catalisador, sinalizado acima da seta:
|
|
MnO2 |
|
|
|
|
2 H2O2(aq) |
\(\longrightarrow \) |
2 H2O(l) |
+ |
O2(g) |
Portanto, o óxido de manganês (MnO2) funciona como um catalizador, ou seja, uma substância que diminui a energia necessária para que uma reação ocorra, deixando o processo bem mais rápido.
Balanceamento de reações químicas
O balanceamento de reações químicas é feito para garantir que o número de átomos de cada elemento seja o mesmo nos reagentes e nos produtos. De certo modo, isso reforça o fato de que a matéria não pode ser criada ou destruída em uma reação química, apenas rearranjada. Sendo assim, veja, a seguir, como é feito o balanceamento:
1. Primeiro, escreva a equação química com os reagentes à esquerda da seta e os produtos à direita. Por exemplo, considere a equação não balanceada para a formação de amônia:
H2 (g) + N2 (g) → NH3 (g)
2. Conte o número de átomos de cada elemento nos reagentes e nos produtos. Dessa forma, temos:
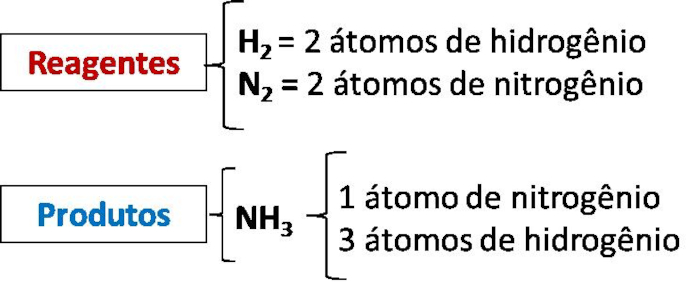
3. Balanceie a equação, adicione coeficientes inteiros antes das fórmulas químicas para ajustar o número de átomos de cada elemento. Diante disso, teremos:
3 H2 (g) + 1 N2 (g) → 2 NH3 (g)
4. Verifique se o número de átomos de cada elemento é o mesmo nos reagentes e nos produtos.
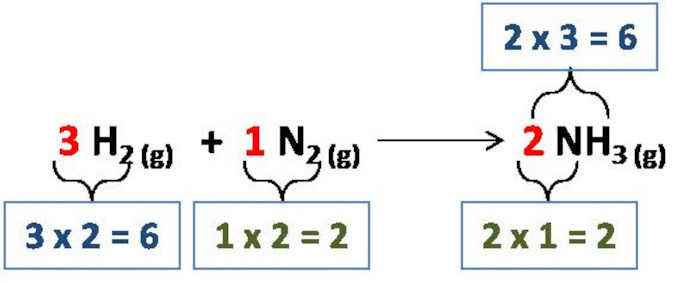
Nesse caso, há agora seis átomos de hidrogênio e dois átomos de nitrogênio em ambos os lados da equação, o que significa que a equação está balanceada.
Qual a importância das reações químicas?
As reações químicas são de extrema importância em diversas áreas da vida cotidiana e da ciência. Afinal, como vimos até aqui, qualquer rearranjo dos átomos para formar novas substâncias se caracteriza como uma reação química, o que nos permite citar centenas de exemplos, entretanto, neste tópico, daremos destaque a alguns pontos que revelam o quão importante elas são.
-
Produção de materiais: são usadas na produção de uma ampla variedade de materiais, desde produtos químicos industriais até medicamentos e materiais de construção. Exemplo: a produção de plásticos, fertilizantes e medicamentos envolve reações químicas.
-
Geração de energia: muitas formas de energia, como a energia elétrica em pilhas e baterias, são produzidas por meio de reações químicas. Ademais, a combustão de combustíveis fósseis para gerar energia térmica e elétrica também é uma reação química.
-
Indústria alimentícia: são essenciais para a produção de alimentos, como fermentação de pães e produção de queijos e bebidas alcoólicas.
-
Processos biológicos: são responsáveis por processos vitais, como a respiração celular, a digestão de alimentos e a produção de energia, no corpo humano e em outros organismos vivos.
-
Meio ambiente: desempenham um papel importante no ciclo de vida dos elementos na natureza, como na fotossíntese (reação química fundamental para a produção de oxigênio) bem como na decomposição de matéria orgânica.
-
Medicina: são usadas para desenvolver novos medicamentos, entender doenças e diagnosticar problemas de saúde por meio de análises químicas.
Portanto, vale ressaltar que as reações químicas fazem parte da nossa existência, logo, compreendê-las e controlá-las é fundamental no desenvolvimento de soluções para problemáticas tanto naturais quanto antrópicas, o que nos permite chegar a novas descobertas e evoluir em tecnologias.
Saiba mais: Como calcular massa, volume, átomos e moléculas em uma reação química
Exercícios resolvidos sobre reações químicas
1) (IFF) Uma reação química ocorre quando há mudanças qualitativas na composição química de substâncias, onde ao menos uma ligação química é criada ou desfeita. Encontramos vários exemplos de reações químicas presentes em nosso cotidiano. Relacione as reações químicas apresentadas com sua classificação (reação de decomposição, simples troca, dupla troca ou síntese).
I. Formação de gás oxigênio a partir da água oxigenada: 2 H2O2 \(\rightarrow\) 2 H2O + O2
II. Formação do óxido de magnésio liberando uma luz branca, que é utilizada nos sinalizadores: 2Mg + O2 \(\rightarrow\) 2MgO
III. Neutralização do ácido clorídrico, presente no suco gástrico, e o hidróxido de alumínio, utilizado como antiácido: 3HCl + Al(OH)3 \(\rightarrow\) AlCl3 + 3H2O
IV. Formação do gás nitrogênio que faz inflar os airbags de automóveis: 2NaN3 \(\rightarrow\) 3N2 + 2Na
Assinale a alternativa que corresponde à classificação correta das reações.
a) decomposição; II. simples troca; III. dupla troca; IV. síntese.
b) síntese; II. simples troca; III. decomposição; IV. síntese.
c) decomposição; II. síntese; III. dupla troca; IV. decomposição.
d) dupla troca; II. simples troca; III. decomposição; IV. síntese.
e) síntese; II. dupla troca; III. dupla troca; IV. simples troca.
Gabarito: C
A decomposição ocorre quando uma única substância dá origem a duas ou mais espécies químicas. Perceba que nos itens “I” e “IV” é exatamente isso que acontece. Logo, por eliminação, já teríamos o nosso gabarito. Contudo, para fins de compreensão, veja que no item “II” acontece o inverso, pois há duas substâncias reagindo para produzirem uma única espécie. Nesse caso, ocorre uma síntese. Por fim, no item “III”, os componentes de cada reagente se separam e trocam seus pares, ou seja, se reagrupam, caracterizando uma dupla troca.
2) (IFPR)Os fertilizantes agrícolas são largamente utilizados para garantir nutrientes aos vegetais, na forma de íons e moléculas, indispensáveis ao crescimento, à floração e à frutificação. Dentre esses fertilizantes, o nitrato de amônio, NH4NO3, é um dos mais empregados na correção do teor de nitrogênio do solo. Esta substância pode ser obtida através da reação entre ácido nítrico e hidróxido de amônio de acordo com a equação:
HNO3 + NH4OH \(\rightarrow\) NH4NO3 + H2O.
Esta reação é classificada como de:
a) síntese.
b) análise.
c) dupla troca.
d) simples troca.
Gabarito: C
Perceba que os reagentes trocam seus pares. O íon NO3- se separa do “H+” e se une ao NH4+, dando origem a um novo composto. Por sua vez, o hidrogênio livre se junta à hidroxila (OH-), formando água (H2O). Portanto, houve uma dupla troca.
Fontes
FELTRE, R. As reações químicas. In: Química Geral. 6. ed. São Paulo: Moderna, 2004. v. 1p. 238–249.
L. BROWN, T. et al. Reações em solução aquosa. In: Química: a ciência central. 13. ed. São Paulo: Pearson Education do Brasil., 2016. p. 124–153.
LOPES, A. R. C. Reações químicas: fenômenos, transformação e representação. Química Nova na Escola, v. 2, p. 7–9, 1995.


