Matéria
Matéria é tudo aquilo que tem massa e volume. É composta por moléculas e átomos unidos e ordenados de diferentes formas, o que garante diferentes propriedades específicas. Também há as propriedades gerais, que são aquelas que se aplicam a todo tipo de matéria.
Matéria e energia são conceitos complementares. A energia, além de unir as partículas formadoras da matéria, está proporcionalmente relacionada a esta. Einstein descreveu matematicamente que matéria e energia são diretamente proporcionais (E=m.c²).
Veja também: Qual é a estrutura de um átomo?
O que é matéria?
A palavra matéria vem do latim e significa “aquilo de que uma coisa é feita”. Matéria é tudo aquilo que possui peso e ocupa espaço no Universo. De acordo com Demócrito, a matéria é formada por pequenas partículas menores, chamadas de átomo, e cada tipo de matéria se distingue pela natureza e forma de organização dos átomos, o que nos leva aos diferentes estados físicos:
-
gasoso;
-
líquido;
-
sólido.
O ar atmosférico que respiramos, por exemplo, também é matéria. Apesar de não conseguirmos ver, o ar tem peso e ocupa espaço. Prova disso é que, quando enchemos um balão, ele ganha volume e, se colocarmos um balão vazio e um cheio em uma balança, poderemos ver que o balão cheio de ar é um pouco mais pesado.

Composição da matéria
A matéria é composta por espécies atômicas ligadas por diferentes forças inter e intramoleculares. Os átomos se organizam e formam moléculas, e as moléculas se unem e formam elementos de dimensões maiores.
A matéria pode ser formada por um tipo apenas de átomo (sendo chamada de substância) ou pode ser formada por dois ou mais átomos, configurando uma mistura.
Leia também: O que são as substâncias simples e compostas?
Tipos de matéria
Podemos classificar a matéria de diversas formas, levando em conta características como:
-
estado físico;
-
natureza do(s) elemento(s) formador(es);
-
origem natural ou artificial;
-
propriedades específicas, etc.
Mas vamos nos ater aqui à matéria orgânica e inorgânica.
-
Matéria orgânica
Matéria orgânica são os compostos que têm em sua estrutura átomos de carbono, realizando ligações covalentes com outros átomos de carbono e com outras espécies atômicas, como:
Todo composto orgânico tem carbonos em sua estrutura, mas nem todo composto que tem carbono é orgânico. Os carbonatos (sais compostos pelo íon CO32−), por exemplo, são compostos inorgânicos.
Antigamente se acreditava que os compostos orgânicos eram exclusivamente produzidos por seres vivos. Em 1828, o cientista Friedrich Wöhler conseguiu, em laboratório, sintetizar a ureia (CH₄N₂O), um composto orgânico, a partir do cianato de amônio (NH4OCN), um composto inorgânico. Depois disso surgiram outros compostos orgânicos sintetizados em laboratório.
-
Inorgânicos
Compostos inorgânicos são normalmente unidos por ligação iônica, como:
São as substâncias que não possuem carbonos ordenados, cadeias de hidrocarbonetos ligadas à molécula. Exemplo de composto inorgânico presente no nosso cotidiano é o cloreto de sódio (NaCl), que é o nosso sal de cozinha. Podemos citar também o hidróxido de sódio (NaOH), também conhecido como soda cáustica.
Propriedades da matéria
Há dois tipos de propriedades da matéria. Aquelas que dizem respeito a todo tipo de matéria são as propriedades gerais, e aquelas que são específicas de uma espécie variam de uma matéria para outra.
-
Propriedades gerais
-
Massa: é a quantidade de matéria que temos em uma determinada amostra. Sua unidade é o quilograma (kg) pelo Sistema Internacional de Unidades (SI).
-
Volume: espaço ocupado pela amostra de matéria. Sua unidade é o m³ pelo SI. Um m³ corresponde a 1000 litros.
-
Impenetrabilidade: toda matéria ocupa um determinado espaço no Universo, e nenhuma outra matéria é capaz de ocupar esse mesmo espaço simultaneamente.
-
Divisibilidade: é possível dividir a matéria em infinitas partes menores até chegarmos às unidades fundamentais da matéria, que hoje sabemos que vão além dos átomos.
-
Descontinuidade: toda matéria é composta por espaços vazios entre os átomos e moléculas.
-
Compressibilidade: capacidade de ter seu volume reduzido por ação de forças externas.
-
Elasticidade: capacidade que a matéria tem de voltar à forma original quando não se tem mais força ou pressão externa agindo sobre ela.
-
Indestrutibilidade: ainda que mude sua estrutura original, a matéria não pode ser destruída. Isso foi afirmado por Lavoisier em sua famosa frase: “nada se cria, nada se perde, tudo se transforma.”
-
Inércia: tendência que um corpo tem de permanecer no seu estado de energia original, seja em repouso, seja em movimento, até que haja a interferência de uma força externa.
Veja também: Primeira lei de Newton – lei da mecânica que comprova a existência da inércia
-
Propriedades específicas
-
Funcionais: propriedades relacionadas com as funções químicas da matéria. É a classificação da matéria conforme a semelhança de funções e reações químicas.
-
Ponto de fusão e ebulição: ponto (temperatura) em que acontece a troca de estado físico da matéria do sólido para o líquido e do estado líquido para o gasoso, respectivamente.
-
Densidade: relação entre massa e o volume que a amostra de matéria ocupa (d=m/v).
-
Solubilidade: capacidade da matéria de se dissolver ou se misturar à outra de forma homogênea.
-
Dureza: capacidade que um material tem de riscar ou cortar outro material.
-
Maleabilidade: capacidade que o material tem de ser moldado sem se partir ou quebrar.
-
Ductibilidade: capacidade de um material de formar fios ou, em outras palavras, até onde suporta ser deformado antes de se romper.
-
Tenacidade: capacidade da matéria de suportar ou absorver impactos sem quebrar.
-
Organolépticas: característica da matéria que podemos observar com os nossos sentidos: tato, visão, audição, olfato e paladar.
Estados físicos da matéria
A matéria pode se apresentar em cinco estados físicos diferentes:
-
condensado de Bose-Einstein;
-
sólido;
-
líquido;
-
gasoso;
-
plasma.
A diferença entre eles é a movimentação e condensação das partículas formadoras.
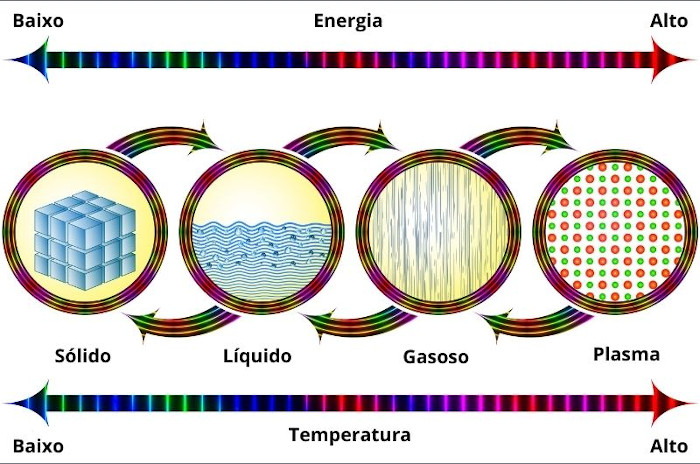
Matéria e energia
A matéria está diretamente relacionada com a energia e vice-versa. Exemplo disso são as forças (energia) que unem as partículas formadoras da matéria, bem como os estados físicos, que aparecem conforme a energia cinética entre as partículas formadoras.
Segundo Einstein, matéria e energia são proporcionais. Ele descreveu isso usando a fórmula matemática:
E = mc²
E → Energia
m → massa
c → velocidade da luz
Assim, se houver aumento de matéria, haverá também aumento da energia associada a ela.
Exercícios resolvidos sobre matéria
Questão 1 – (Osec – SP) Densidade é uma propriedade definida pela relação:
A) massa/pressão.
B) massa/volume.
C) massa/temperatura.
D) pressão/temperatura.
E) pressão/volume.
Resolução
Alternativa B. Densidade é a relação de massa que se tem em um determinado volume. É determinada pela fórmula d=m/v.
Questão 2 – Você está sentado no interior de um ônibus em movimento. De repente, ele freia bruscamente e você é projetado violentamente para frente. Isso ocorre graças à propriedade geral da matéria denominada:
A) densidade.
B) impenetrabilidade.
C) elasticidade
D) inércia.
E) volume.
Resolução
Alternativa D. Inércia é a tendência de qualquer matéria de se manter em seu estado de energia cinética até que haja interferência de uma força externa. O estado de energia do passageiro era em movimento, pois o ônibus que o levava estava em movimento. Quando o ônibus freia, ele impõe uma força para que o corpo pare de se movimentar. Com isso, o passageiro é projetado para frente porque a tendência é que tudo que está dentro do ônibus se mantenha no movimento que o ônibus fazia antes de ser freado.
Questão 3 – Em condições normais, o ponto de ebulição da água é 100 °C. Podemos afirmar que essa é uma propriedade:
A) específica.
B) genérica.
C) funcional.
D) geral.
E) organoléptica.
Resolução
Alternativa A. É uma propriedade específica, pois cada tipo de matéria possui um ponto de ebulição diferente, de acordo com a natureza, estrutura e massa do composto.

