Carbonila (CO)
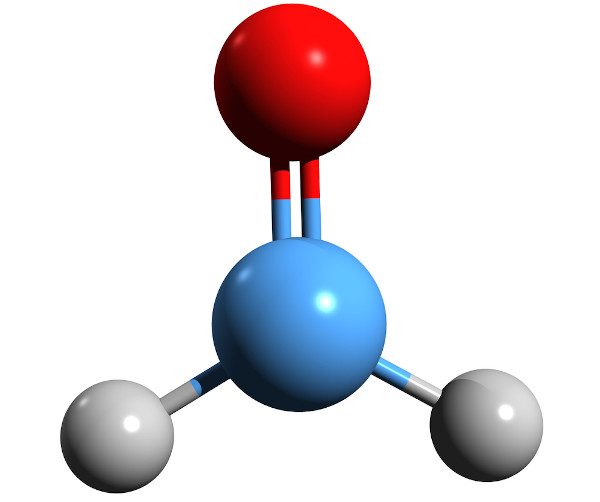
A carbonila é um grupo funcional formado pela ligação dupla entre um átomo de carbono e de oxigênio (C=O). Muitos grupos funcionais orgânicos possuem a carbonila em sua estrutura, como cetonas, aldeídos, ácidos carboxílicos, amidas, entre outros.
O átomo de carbono da carbonila possui hibridização sp2 e mantém geometria molecular trigonal plana. A presença da carbonila na estrutura interfere em propriedades da molécula, como polaridade e pontos de fusão e de ebulição.
Leia também: Funções orgânicas — as substâncias que apresentam propriedades químicas semelhantes
Resumo sobre carbonila
- O grupo carbonila é formado por um átomo de carbono e um de hidrogênio, unidos por ligação dupla.
- Muitas funções orgânicas contêm o grupo carbonila, como aldeídos, cetonas, ácidos carboxílicos, ésteres etc.
- O grupo carbonila possui geometria trigonal plana e hibridização sp2 no carbono.
- A presença da carbonila na molécula altera algumas propriedades físico-químicas, como polaridade e ponto de ebulição.
O que é a carbonila?
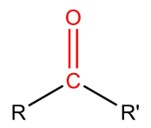
A carbonila é um grupo funcional formado por um átomo de carbono ligado a um átomo de oxigênio por uma ligação dupla, sendo representado por C=O ou CO. Na imagem, os grupos R e R’ são substituintes do carbono.
Há muitas classes de compostos orgânicos que contêm o grupo carbonila e são denominados compostos carbonílicos, como cetonas, aldeídos e ácidos carboxílicos.
O grupo carbonila também está presente em alguns compostos inorgânicos, na forma do ligante monóxido de carbono (CO).
Estrutura da carbonila
Na carbonila, o átomo de carbono possui hibridização sp2 e, portanto, a carbonila possui geometria trigonal plana, com ângulos de ligação de 120°.
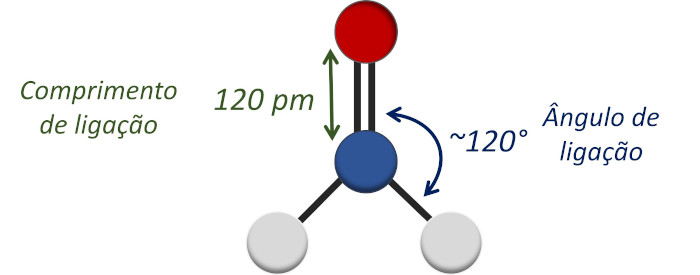
Em compostos orgânicos, o comprimento da ligação C=O se mantém próximo a 120 picômetros (pm). Em compostos inorgânicos, o comprimento da ligação tende a ser menor.
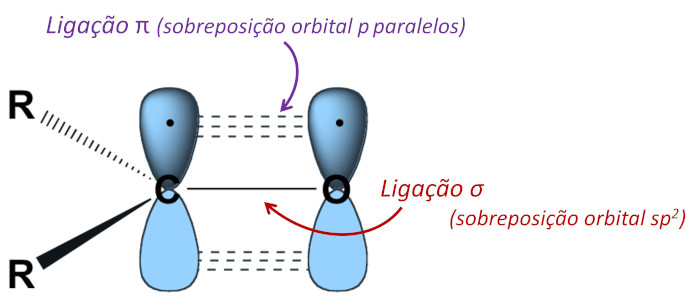
Dos três orbitais sp2 do carbono, um deles se sobrepõe ao oxigênio, formando a ligação sigma (Ω). O orbital 2p não hibridizado do carbono é perpendicular ao plano da ligação sigma, ficando “lado a lado” com o orbital 2p do oxigênio, estabelecendo, dessa forma, a ligação pi (π).
Para que serve a carbonila?
A presença do grupo carbonila em compostos carbonílicos altera algumas de suas propriedades, como polaridade, reatividade e pontos de fusão/ebulição.
Em razão das diferentes eletronegatividades, o átomo de oxigênio possui maior afinidade por elétrons, atraindo para si o par de elétrons da ligação dupla e gerando uma densidade de carga positiva sobre o átomo de carbono pela “falta de elétrons”. Em razão dessa separação de cargas, o grupo carbonila é polar.
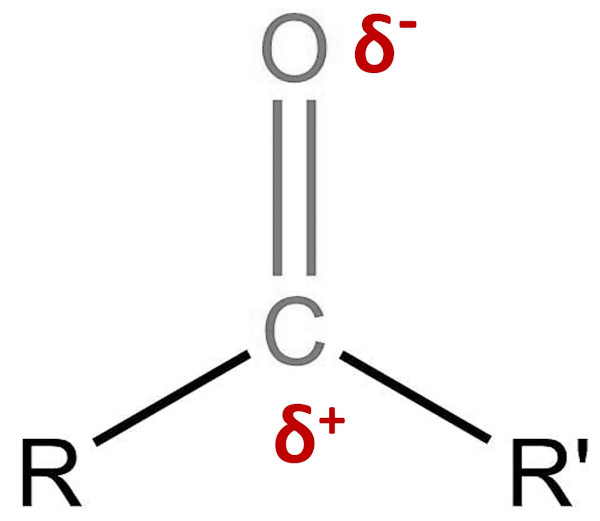
Assim, os compostos carbonílicos também são polares e, em razão disso, possuem pontos de fusão e de ebulição mais elevados do que os respectivos hidrocarbonetos de mesmo número de carbonos.
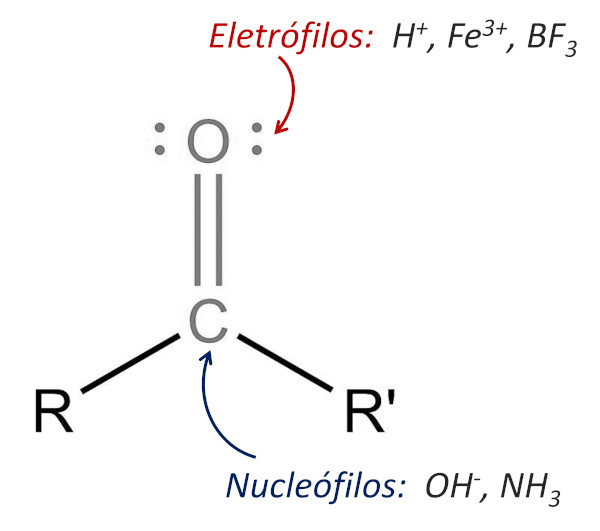
A reatividade também é afetada pela presença do grupo carbonila, uma vez que o átomo de carbono interagirá com reagentes ricos em elétrons (nucleófilos) e o átomo de oxigênio terá maior afinidade com reagentes que possuam deficiência de elétrons (eletrófilos).
Compostos com o grupo carbonila
Na química orgânica, o grupo carbonila compõe a estrutura básica de diferentes classes de compostos, conhecidos como carbonílicos ou carbonilados.
-
Aldeídos
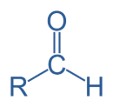
Aldeídos são caracterizados pela ligação da carbonila a, pelo menos, um átomo de hidrogênio. Em razão dessa configuração, o grupamento aldeído sempre está posicionado na extremidade da cadeia carbônica.
-
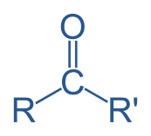
Cetona
Em cetonas, a carbonila está posicionada entre duas cadeias carbônicas, ocupando sempre uma posição no interior da cadeia e nunca nas extremidades.
-
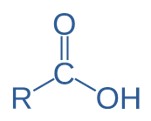
Ácido carboxílico
Em ácidos carboxílicos, a carbonila está ligada a uma cadeia carbônica e uma hidroxila (grupamento -OH). Em razão dessa configuração, o grupo ácido carboxílico sempre está nas extremidades da cadeia.
-
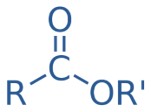
Éster
Os ésteres são derivados de ácidos carboxílicos, em que o átomo de oxigênio do grupo hidroxila se liga a uma cadeia carbônica, e não mais ao átomo de hidrogênio, tornando essa cadeia heterogênea. Nos ésteres, o grupo carbonila se encontra no interior da cadeia carbônica.
-
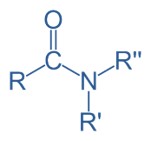
Amida
Nas amidas, o grupo carbonila está ligado ao átomo de nitrogênio. As amidas são derivadas do ácido carboxílico pela reação com as aminas. Por meio dessa reação, formam-se os aminoácidos, os blocos de construção das proteínas.
-
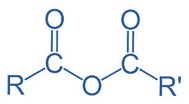
Anidrido
Os anidridos são formados pela união de duas moléculas de ácido carboxílico, assim, a estrutura dos anidridos possui dois grupos carbonila.
-
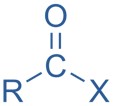
Haletos ácidos
Os haletos ácidos são derivados dos ácidos carboxílicos e possuem o grupo carbonila ligado a um halogênio (flúor, cloro, bromo, iodo).
Carbonila x carboxila
Carboxila é o termo utilizado para se referir ao grupo funcional formado pelo grupo carbonila e por uma hidroxila, semelhante ao grupo funcional que caracteriza o ácido carboxílico. Assim, podemos dizer que:
- Carbonila se refere à ligação entre carbono e oxigênio por uma dupla ligação.
- Carboxila, dessa forma, contém uma carbonila em sua estrutura.
A imagem abaixo destaca essas duas estruturas.
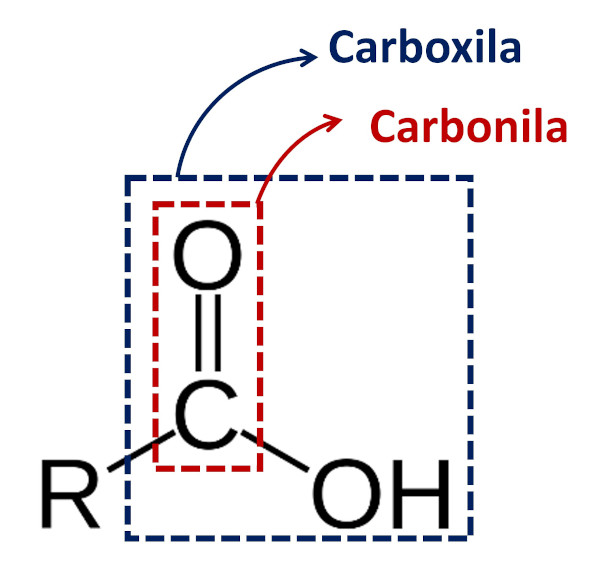
A Iupac, atualmente, adota apenas o termo grupos carbonílicos para englobar os grupos funcionais que contêm o grupamento C=O.
Leia também: Funções oxigenadas — os compostos formados pelo elemento oxigênio
Exercícios resolvidos sobre carbonila
Questão 1
(UEA) São apresentadas as estruturas de três compostos que apresentam em comum o grupo carbonila no centro da estrutura.
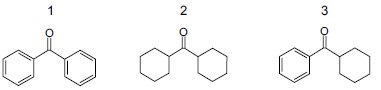
Nas estruturas 1, 2 e 3, encontra-se o grupo funcional característico da função orgânica:
a) éter
b) aldeído
c) cetona
d) amida
e) éster
Resolução: Letra C
As três estruturas apresentam o grupo carbonila (C=O) dentro de cadeias carbônicas, caracterizando o grupo funcional cetona.
Questão 2
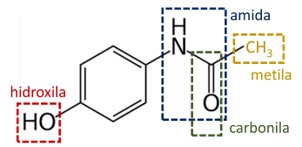
(UFMG) O paracetamol, empregado na fabricação de antitérmicos e analgésicos, tem esta estrutura:
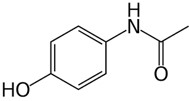
É INCORRETO afirmar que, entre os grupamentos moleculares presentes nessa estrutura, se inclui o grupo
a) amino.
b) carbonila.
c) hidroxila.
d) metila.
Resolução: Letra A
A imagem abaixo destaca os grupos funcionais presentes na estrutura do paracetamol. Note que, entre as alternativas, apenas o grupo amino não faz parte da estrutura.