Íons
Íons são espécies atômicas formadas quando uma espécie eletricamente neutra perde ou ganha elétrons. Dessa forma, podem ser tanto carregados positivamente, sendo chamados de cátions, ou carregados negativamente, sendo chamados de ânions. A carga do íon gerado será numericamente igual ao número de elétrons recebidos ou perdidos pela espécie.
Os íons são formados durante processos reacionais, sendo que a propensão a se tornarem cátions ou ânions dependerá de duas grandezas: a energia de ionização e a afinidade eletrônica. Em geral, metais tendem a se tornar cátions e ametais tendem a se tornar ânions.
Veja também: Raio iônico — a relação entre o aumento e a diminuição do átomo quando ele perde ou ganha elétrons
Resumo sobre os íons
-
Íons são formados quando uma espécie eletricamente neutra perde ou ganha elétrons.
-
Se há perda de elétrons, o íon gerado é positivo, sendo chamado de cátion.
-
Se há ganho de elétrons, o íon gerado é negativo, sendo chamado de ânion.
-
Os íons são formados durante processos reacionais, como na clivagem de uma ligação covalente.
-
A energia de ionização e a afinidade eletrônica são grandezas importantes para avaliar se uma espécie é mais propensa a ser um ânion ou um cátion.
-
Íons podem se ligar por meio de uma junção química chamada de ligação iônica, de grande força e atração.
Videoaula sobre íons
O que são íons?
Um íon é uma espécie atômica eletricamente carregada, seja positivamente (cátion) ou negativamente (ânion). São formados quando espécies eletricamente neutras ganham ou perdem elétrons em processos reacionais.
Em geral, um íon pode ser simples ou composto. Os íons simples são aqueles formados por um único elemento químico, enquanto o íon composto é aquele formado por dois ou mais elementos químicos, como é possível perceber nos exemplos a seguir.
-
Íons simples: Na+, Fe3+, O2-, Cl-.
-
Íons compostos: PO43-, SO32-, NH4+.
Para que servem os íons?
Os íons, por serem eletricamente carregados, têm a capacidade de tornar as soluções condutoras de corrente elétrica, as quais são chamadas de soluções eletrolíticas. É a partir da compreensão dessas soluções que dispositivos de geração de energia elétrica, como as pilhas, foram desenvolvidos.

A exploração dos íons também tem grande importância em processos de separação. As resinas de troca iônica são amplamente utilizadas em laboratórios, onde um composto faz a substituição de um íon de sua estrutura por outro da solução de mesma carga, fazendo a remoção deste íon.
Classificação dos íons
Um íon pode ser carregado positivamente ou negativamente, a depender se a espécie ganhou ou perdeu elétrons. Assim, podem ser classificados como:
-
Cátions: íons positivos, gerados a partir da perda de elétrons.
X → Xn+ + n e-
-
Ânions: íons negativos, gerados a partir do ganho de elétrons.
Y + n e- → Yn-
Como se formam os íons?
Os íons são formados por meio de processos químicos. O principal deles é a ionização, uma reação química em que energia suficiente é colocada para retirar um ou mais elétrons da camada de valência do átomo neutro. A energia necessária para a retirada do elétron é conhecida como energia de ionização.
Os metais são conhecidos por possuírem baixa energia de ionização, o que significa que possuem grande tendência a perderem elétrons e se tornarem cátions. Por exemplo, são necessários 496 kJ de energia para se retirar os elétrons de valência de um mol de átomos de sódio, formando-se o cátion Na+.
Na + 496 kJ → Na+ + e-
Também é considerada uma reação de ionização a cisão heterolítica de uma ligação covalente, ou seja, uma ruptura em que todos os elétrons da ligação migram para um átomo, gerando um cátion e um ânion, como ocorre na dissolução do cloreto de hidrogênio, HCl.
HCl → H+ + Cl-
Os ânions são formados quando elétrons são inseridos na estrutura atômica. A tendência de um átomo se tornar um ânion é mensurada pela afinidade eletrônica, a energia liberada pela espécie ao receber um elétron. Quanto mais energia liberada, mais aceito pela estrutura é o elétron. Quando elétrons são inseridos na estrutura de um mol de átomos de cloro, por exemplo, há a liberação de 349 kJ de energia.
Cl + e- → Cl- + 349 kJ
Diferenças entre íons, átomos e moléculas
Embora sejam completamente diferentes, os conceitos de íons, átomos e moléculas podem causar confusão em estudantes que estão iniciando seus estudos em Química. Os átomos são os constituintes da matéria, eletricamente neutros, formados basicamente por prótons, nêutrons e elétrons. Quando se ligam por meio de uma ligação química covalente, os átomos dão origem às moléculas. Por isso, compostos covalentes e moléculas são sinônimos.
Já os íons são formados quando átomos (ou até mesmo moléculas) perdem ou ganham elétrons. Isso porque os elétrons estão na região periférica do átomo, a eletrosfera, sendo facilmente retirados ou inseridos na estrutura.
Leia também: Atomística — a área da Química responsável pelo estudo do átomo
Ligação iônica
Íons de cargas opostas podem se ligar por meio de atrações eletrostáticas, conhecidas na Química como ligação iônica. Os compostos iônicos possuem, então, uma parte negativa (ânion) e uma parte positiva (cátion), mantidas por uma forte atração entre cargas opostas. Nessa modalidade de ligação, um elemento de baixa energia de ionização (metal) perde elétrons para um elemento de alta afinidade eletrônica (ametal).
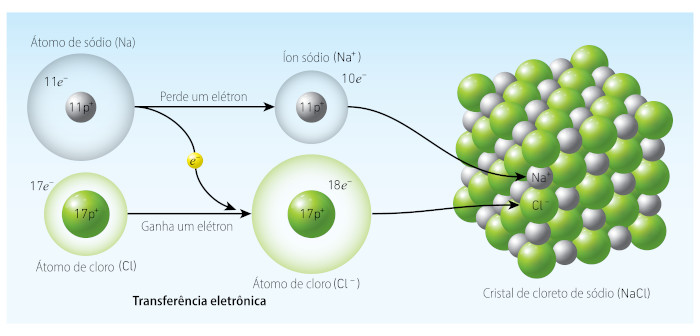
O que chama a atenção nos compostos iônicos é que a forte atração entre as cargas gera estruturas cristalinas bem ordenadas geometricamente. Outra consequência dessa forte atração é que os compostos iônicos acabam se apresentando como sólidos em temperatura ambiente.
Exercícios resolvidos sobre íons
Questão 1
(Colégio Naval, 2017) O elemento químico Al (alumínio), largamente utilizado em utensílios domésticos, tem número atômico 13, número de massa 27, e seu íon Al3+ é muito utilizado no solo. Assinale a opção que apresenta, respectivamente, o número de prótons, elétrons e nêutrons presentes no íon Al3+.
A) 13, 10, 14.
B) 10, 10, 14.
C) 13, 13, 27.
D) 10, 10, 27.
E) 13, 16, 14.
Resolução: Alternativa A
Se a espécie iônica é Al3+, entende-se que é um cátion e foi formado a partir da perda de três elétrons. Assim, como o átomo de alumínio possui 13 elétrons, o íon de alumínio possui apenas dez. Os nêutrons e prótons permanecem inalterados. O número de nêutrons pode ser calculado pelo número de massa (A):
A = Z + n
27 = 13 + n
n = 14
Questão 2
(PUCCamp-SP 2009) O símbolo para o íon cálcio, Ca2+, indica que
I. é um ânion.
II. possui dois prótons a mais que o respectivo átomo neutro.
III. perdeu dois elétrons em relação ao átomo neutro.
Está correto o que se afirma SOMENTE em:
A) I.
B) II.
C) III.
D) I e II.
E) II e III.
Resolução: Alternativa C
O íon Ca2+ é positivo, o que indica que é um cátion, formado a partir da perda de dois elétrons de seu átomo neutro. Nesse processo, o número de prótons se mantém intacto, portanto, não se altera. Dessa forma, apenas a terceira afirmativa está correta.


